术后认知功能障碍(postoperative cognitive dysfunction,POCD)是手术麻醉后患者出现记忆力、执行能力及定向力等方面的障碍,同时伴有社会活动能力减退的一种常见的神经系统并发症。POCD属于更名后“围术期神经功能障碍”(perioperative neurocognitive disorders,PND)的研究范畴。老年人术后发生率为10%~54%[1-4],对患者术后恢复及生活质量影响大,给社会及家庭造成沉重的经济负担,目前已经成为重要的公共卫生问题[5-6]。但迄今为止,POCD的发病机制尚不明确,诊断主要依赖于一系列神经心理学量表测试[7],该方法耗时长、主观性强、患者配合度低。因此,当用于大样本的临床研究以及繁忙的临床工作时,该评估工具存在明显不足[8]。
近年随着神经影像学的发展,特别是磁共振成像(magnetic resonance imaging,MRI),以非侵入性测量神经活动及捕获详细的人类大脑图像为特征[9],不仅促进了神经精神疾病的解剖功能学研究,也为寻找POCD的客观诊断标准带来了新思路。非对比剂增强动脉自旋标记(arterial spin-labeling,ASL)灌注成像可描述认知完好的老年患者基线访视时脑灌注的早期和细微变化,该信息可用于预测随后认知减退的早期阶段[10]。目前,使用ASL评估POCD的研究尚未见报道。本研究旨在观察比较老年POCD患者术前局部脑血流(region cerebral blood flow,rCBF)变化,并进一步研究其与患者神经精神量表结果是否存在相关性。
资料和方法研究对象 本研究经上海市同济医院伦理委员会批准(ChiCTR-DDD-17010762),患者或其家属签署知情同意书。选取2017—2020年在上海市同济医院择期行脊柱手术的患者,入选标准:(1)年龄≥65岁,(2)ASA Ⅰ~Ⅱ级。排除标准:(1)简易精神量表(mini-mental tate examination,MMSE)评分 < 20分或者诊断为轻度认知功能损害(mild cognitive impairment,MCI);(2)先前存在神经和/或精神疾病(如帕金森病);(3)心脏和/或中枢神经系统血管疾病史;(4)听觉障碍、视力或语言障碍,阻碍交流;(5)不适合MRI检查的情况(如幽闭恐怖症);(6)无法配合术前和术后的认知功能评估;(7)术中出血量 > 600 mL;(8)手术时间 > 6 h。根据术后是否发生POCD将患者分为POCD组和非POCD组。
麻醉方法 术前常规禁饮禁食,入室常规心电监护,开放外周静脉通路。麻醉诱导采用舒芬太尼(0.2~0.3 μg/kg)、依托咪酯(0.3 mg/kg)、顺式阿曲库铵(0.15 mg/kg)静推,1 min后可视喉镜引导下气管内插管。设置机械通气参数为潮气量8~10 mg/kg,呼吸频率设置为10~12次/min,吸入氧流量为2 L/min,I:E 1∶2,吸入氧浓度40%~60%,其中呼气末二氧化碳(PETCO2)保持在(35±5)mmHg(1 mmHg=0.133 kPa,下同)。麻醉维持采用静吸复合麻醉,术中丙泊酚、瑞芬太尼持续微泵,根据麻醉深度辅助吸入七氟醚。术中备用阿托品与麻黄碱调控血压与心率;另外根据脑电双频指数(bispectral index,BIS)调节麻醉深度,维持在40~60。术后进行患者自控静脉镇痛;我们用0~10的视觉模拟评分(0表示没有疼痛,10表示能想象到的最疼的疼痛)来评估患者术后疼痛。
认知功能评定 经过专业培训的评估者分别在术前1天及术后7天由同一评估者对患者进行认知功能评定,进行评定时需要在安静的房间且只有患者及评估者在场,且评估者对患者的病情及检查结果不知情。评定方法包括简易精神量表(Mini-Mental State Examination,MMSE),蒙特利尔认知评估(Montreal Cognitive Assessment,MoCA),连线测试(Trail Making Test,TMT),雷伊听觉语言学习测试(Rey Auditory Verbal Learning Test,AVLT),Stroop颜色单词实验(Stroop Colour Word Test,STROOP),数字符号替换测试(Digit Symbol Substitution Test,DSST),本顿线方向判断实验(Judgment of Line Orientation Test,JLOT),视觉空间记忆测试(Brief Visuospatial Memory Test-revised,BVMT immediate and delayed),语义流畅性(Semantic Fluency Test,SFT),数字广度测试(Digit Span Test,DST)。此外,术后每天直到出院当天都会由一名专业培训的评估人员对患者进行谵妄评估量表(Confusion Assessment Method,CAM)评估[11-12]。
POCD诊断标准 采用ISPOCD研究协作组推荐的综合评分法,即“Z计分法”。为排除神经心理学的假阳性率,排除学习效应,收集20例正常参照人群,并测试出正常参照人群间隔相同时间内每项测试的差值μ及标准差δ,将每个患者术前术后每个测试项目的差值x减去正常人群的对应测试项目的差值μ,再与正常人群的平均标准差δ相除得出每个单项测试的Z值,即公式:Z=(x-μ)/δ。符合2个以上单项测试的|Z|值≥1.96,可定义为该患者发生了POCD。Z计分法是对总体认知功能进行评价,排除了封顶效应。
MRI检查及数据预处理 我们使用同济大学附属同济医院(中国上海)三维磁化制备的快速梯度回波(3D-mprage)序列,配备32通道头线圈。所有符合纳入标准的患者都在术前1天用3.0-T MRI扫描仪(Verio,德国Siemens公司)完成扫描。过程中患者取仰卧位,闭上眼睛,避免思考任何事情;在扫描前禁食至少4 h,扫描当天禁止服用血管活性药物。ASL使用背景抑制的2D采集脉冲式标记ASL(pASL)序列获得,标记方法采用近端反转控制偏共振效应(proximal inversion with a control for off-resonance effects,PICORE)。具体参数如下:TR=3 500 ms,TE=15 ms,翻转角度90°;层厚=3.5 mm,没有层间距,FOV=224 mm×224 mm,矩阵=64×64,标记时间=700 ms,标记后延迟时间=1 800 ms,激励次数=1,层数=33,总扫描时间=331 s,ASL成像采集91组图像,其中一组为M0,其余90组为PASL图像(包括成对的一组标记像和控制像)。标记像对流入的血液进行标记,控制像对流入血液进行正反两个方向标记,即效果相当于没有标记。用控制像减去标记像即得到颅脑灌注图。
使用全脑获取高分辨率T1加权图像三维脑容量成像MPRAGE序列,参数如下:TR=2 530 ms,TE=2.98 ms,倒置时间=450 ms,翻转度=7°,层厚=1 mm,没有层间距,FOV=256 mm×256 mm,矩阵大小=256×256,体素大小=1 mm×1 mm×1 mm,层数=192,总扫描时间=363 s。
使用基于Matlab R13b的SPM8和ASLtbx工具包,脑成像工具包(DPABI,http://www.restfmri.net)进行数据预处理和分析。使用基于SPM8(http://www.fil.ion.ucl.ac.uk/spm)的工具箱ASLtbx对每个受试者进行图像预处理。处理步骤包括运动校正、配准,空间平滑、去除颅外体素,CBF量化、部分体积校正和空间登记到蒙特利尔神经学研究所(MNI)标准脑空间。
统计学方法 采用SPM8软件包对上述步骤得到的POCD患者组和正常对照组的标准化脑灌注图像进行统计建模及模型评估。以各受试者的年龄、性别为协变量进行统计分析,排除全脑灌注的个体差异。两组间差异比较采用双样本t检验。为控制统计分析的假阳性比例,减少Ⅰ类错误,采用高斯随机场(Gauss random field,GRF)原理的FWE进行多重比较校正,得到有统计学差异的脑区(FWE群集级校正,P < 0.05;体素水平校正,P < 0.001)。
本研究使用SPSS 21.0(IBM,USA)对所得数据进行统计分析。定量资料中,正态分布数据以x±s表示,而非正态分布数据以中位数和四分位数间距(IQR)表示;分类数据以数字和百分比表示;组间分类数据的分析采用χ2检验或Fisher检验。定量资料分析采用双样本t检验或Wilcoxon检验。P < 0.05为差异有统计学意义。
选取ASL组间差异分析中获得的聚类进行临床神经精神量表的进一步分析。提取聚类的CBF值,作为区域平均脑血流分布。对每个脑区进行潜在混杂因素调整后,使用SPSS 21.0对CBF和NPT评分进行Pearson相关性分析。P < 0.05为差异有统计学意义。
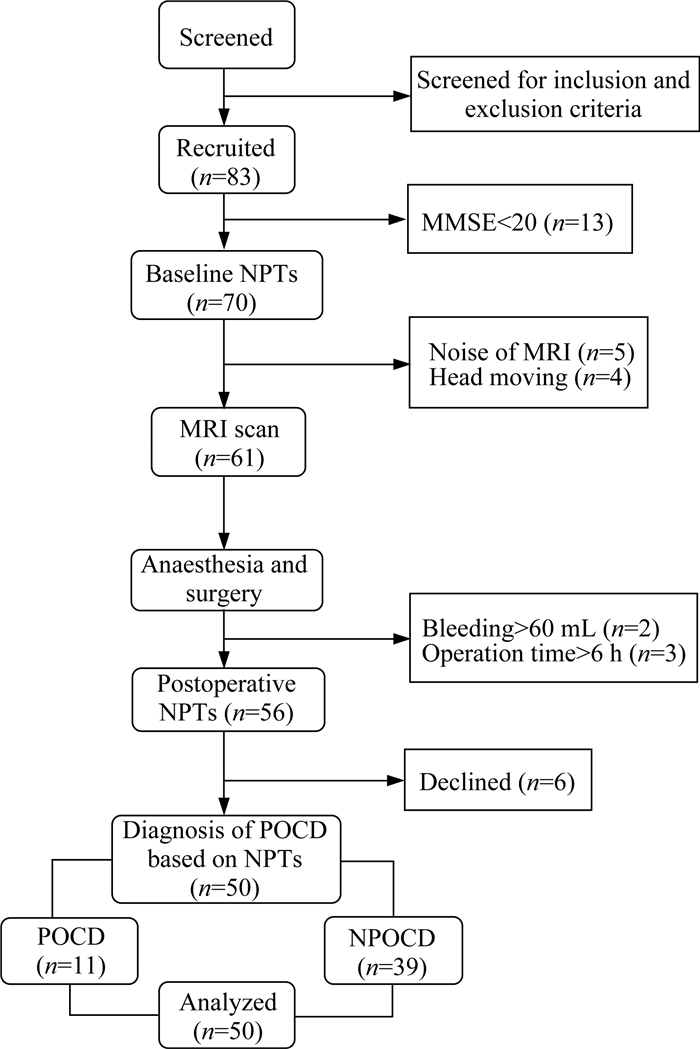
结果患者的基本临床特征 本研究初始纳入83例患者,13例患者因MMSE < 20分而排除,5例患者因无法耐受核磁噪音而拒绝行MRI检查,4例患者因检查中剧烈头动而排除,2例患者因术中出血量 > 600 mL而排除,3例患者手术时间 > 6 h而排除。6例患者因术后拒绝配合认知功能评定而剔除出本研究,最终纳入50例患者,脊柱手术老年患者早期POCD发生率为11例(22%),具体见图 1。患者的一般特征和临床特征见表 1。POCD患者平均年龄为(68.0±2.4)岁,而NPOCD患者平均年龄为(71.0±5.5)岁,其他临床特征差异无统计学意义。
|
| NPTs: Neuropsychological tests. 图 1 试验流程图 Fig 1 Flow diagram for study assessments |
| Characteristics | POCD(n=11) | NPOCD(n=39) | Statistical value | P |
| Age(y) | 68(2.4) | 71(5.5) | 7.560a | 0.013 |
| Gender(M/F) | 5/6 | 18/21 | 0.003a | 0.636 |
| Height(cm) | 168.81 | 163.75 | 0.562a | 0.133 |
| Weight(kg) | 67.72 | 67.00 | 0.370a | 0.842 |
| Education(y) | 8.36(3.0) | 9.10(3.2) | 0.237a | 0.514 |
| Comorbidities | ||||
| COPD(%) | 0(0) | 1(2.9) | 0.297b | 0.771 |
| Cardiopathy(%) | 0(0) | 1(2.9) | 0.608b | 0.590 |
| Diabetes(%) | 2(18.2) | 5(22.7) | 0.412b | 0.420 |
| Hypertension(%) | 2(18.2) | 15(38.4) | 1.939b | 0.144 |
| Intraoperative conditions | ||||
| Surgical duration(min) | 161.36(140.00-205.00) | 183.33(136.25-227.50) | -1.216c | 0.224 |
| Anesthesia duration(min) | 197.27(190.00-225.00) | 228.87(170.00-277.50) | -1.510c | 0.131 |
| Bleeding volume(mL) | 200.00(100.00-300.00) | 200.00(100.00-325.00) | -0.439c | 0.661 |
| BIS | 53.82(53.00-57.00) | 53.00(53.00-56.00) | -0.534c | 0.594 |
| Visual analogue score | 2.29(1.00-3.00) | 2.21(2.00-3.00) | -1.693c | 0.091 |
| Ramsay score | 1.36(1.00-2.00) | 1.41(1.00-2.00) | -0.246c | 0.806 |
| aF;b Fisher;c Z.BIS:Bispectral index. | ||||
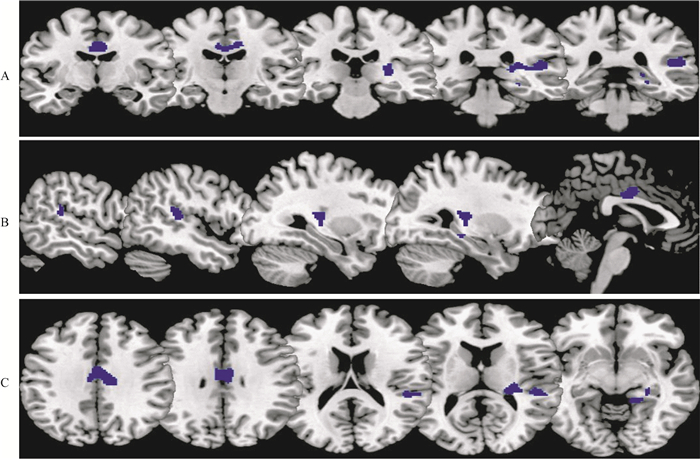
影像学与量表结果 与NPOCD组相比,POCD组术前MRI扣带回CBF显著降低(图 2);扣带回CBF与神经精神量表JLOT、BVMT-D、DST-B的Z分的相关系数(r值)分别为-0.631、-0.480、-0.533,差异具有统计学意义(P < 0.05)。
|
| Voxel-based comparison superimposed onto Montreal Neurologic Institute standard brain in the coronal (A), axial (B), and sagittal planes (C). 图 2 POCD组与NPOCD组术前扣带回脑血流差异 Fig 2 Differences in preoperative CBF in cingulate between POCD and NPOCD patients |
近年来,MRI技术已成为研究POCD病因机制及发生发展的重要手段[9-10, 13],MRI在了解神经系统疾病方面具有明显优势。其中ASL提供了主要血管和组织灌注情况,已成为各种认知功能减退疾病的重要辅助诊断[14-18]。然而,使用ASL研究POCD的报道目前尚少,更缺乏ASL用于POCD的辅助诊断与神经精神量表的相关性研究。本研究旨在观察POCD患者术前CBF的变化及术前CBF与神经精神量表结果的相关性。结果发现,与NPOCD患者比较,POCD患者术前MRI扣带回脑CBF显著降低,且与神经精神量表结果之间有显著的相关性。
POCD患者术前MRI扣带回脑rCBF显著降低 扣带回属于边缘系统,是情绪、行为和记忆的中心。它由一组复杂的结构组成。扣带回具有结构与行为功能的复杂多样性,因此与许多脑部疾病的发生都有密切关系[19]。
目前已有研究表明扣带回的CBF下降与认知功能受损密切相关。Yoshida等[20]报道在AD早期,扣带回CBF就明显减少。此外,Johnson等[17]也证明了从MCI转化为AD的患者中扣带回灌注是降低的。这些均表明,脑血流减少是早期认知功能障碍的敏感标志。我们观察到,POCD组患者术前神经心理测试评估表现正常,但是术前扣带回的CBF却已经出现明显下降,我们认为这可能与神经认知储备有关。由于不同个体的易感性、受教育程度和社会参与度不同,有些人可以代偿性维持相对正常的认知功能。Xekardaki等[21]发现由于神经认知储备的激活,认知功能退化患者虽然前期可以维持正常的认知,但和MCI患者在基线水平具有相似的脑血流改变,说明他们在此时已经有脑血流灌注变化。因此我们推测:POCD的受试者虽然术前已出现扣带回脑血流下降,但由于认知储备的原因能够弥补CBF的变化,以维持正常的认知功能状态。但是,手术和麻醉可能加速POCD患者认知储备的耗竭,进而出现认知恶化。
术前扣带回CBF与神经精神量表结果之间具有显著的相关性 实验结果发现术前扣带回CBF与神经精神量表JLOT、BVMT-D、DST-B结果具有显著相关性;这3个量表广泛应用于儿童和成人的认知评估,均侧重评估记忆力或注意力。JLOT用来测量空间思维,是用于评估脑损伤患者右半球功能的临床评估工具[22];BVMT主要测试视觉空间学习和记忆任务;数字广度测试(DST)评估注意力和记忆力。研究表明,扣带回认知亚区通过影响感觉或反应选择,调节注意或执行功能,包括监测竞争、复杂运动控制、动机、新奇、错误监测、工作记忆和认知任务的预期等。由此看来,术前扣带回CBF与神经精神量表都可以用来评估POCD患者认知功能(注意力、记忆力),且二者结果具有良好的相关性。
众所周知,POCD的早期诊断具有重要意义,目前诊断主要依赖于神经心理学测试,尚无统一诊断标准。不同的研究人员对POCD的诊断应用不同的量表和组合,缺乏准确性,增加了误诊、漏诊概率,并且可能过高估计了POCD的发生率,这不仅影响POCD患者的早期诊断和预后,也为POCD的研究带来了困扰。本研究发现POCD组扣带回CBF与神经精神量表JLOT、BVMT-D、DST-B的Z分的具有显著相关性。这3个量表应当是比较适合POCD随访研究的认知测试。
综上所述,老年POCD患者术前MRI扣带回脑CBF显著降低,提示术前CBF值有助于老年手术患者早期POCD的预测;且CBF与神经精神量表结果之间具有良好的相关性。
作者贡献声明 杜雪 论文构思撰写和修订,临床数据采集。刘苏,杨君君 数据统计。高燕 影像数据处理。张静亚 临床数据采集。刘健慧 临床研究设计,论文指导。
利益冲突声明 所有作者均声明不存在利益冲突。
| [1] |
DEEPAK B, GOLDHAMMER JE, SPERLING MR, et al. Cognitive outcomes after coronary artery bypass grafting[J]. J Cardiothorac Vasc Anesth, 2017, 31(2): 707-718.
[DOI]
|
| [2] |
JACOB S, CHRISTENSEN KB, LUND T, et al. Long-term consequences of postoperative cognitive dysfunction[J]. Anesthesiology, 2009, 110(3): 548-555.
[DOI]
|
| [3] |
ANDROSOVA G, KRAUSE R, WINTERER G, et al. Biomarkers of postoperative delirium and cognitive dysfunction[J]. Front Aging Neurosci, 2015, 7: 112.
|
| [4] |
MOLLER JT, CLUITMANS P, RASMUSSEN LS, et al. Long-term postoperative cognitive dysfunction in the elderly ISPOCD1 study.ISPOCD investigators.International Study of Post-Operative Cognitive Dysfunction[J]. Lancet, 1998, 351(9106): 857-861.
[DOI]
|
| [5] |
POLUNINA AG, GOLUKHOVA EZ, GUEKHT AB, et al. Cognitive dysfunction after on-pump operations: neuropsychological characteristics and optimal core battery of tests[J]. Stroke Res Treat, 2014, 2014: 302824.
|
| [6] |
DUAN X, ZHU T, CHEN C, et al. Serum glial cell line-derived neurotrophic factor levels and postoperative cognitive dysfunction after surgery for rheumatic heart disease[J]. J Thorac Cardiovasc Surg, 2018, 155(3): 958-965.
[DOI]
|
| [7] |
NEEDHAM MJ, WEBB CE, BRYDEN DC. Postoperative cognitive dysfunction and dementia: what we need to know and do[J]. Br J Anaesth, 2017, 119(suppl_1): i115-i125.
|
| [8] |
SHAIK MA, CHAN QL, XU J, et al. Risk factors of cognitive impairment and brief cognitive tests to predict cognitive performance determined by a formal neuropsychological evaluation of primary health care patients[J]. J Am Med Dir Assoc, 2016, 17(4): 343-347.
[DOI]
|
| [9] |
NANBA T, OGASAWARA K, NISHIMOTO H, et al. Postoperative cerebral white matter damage associated with cerebral hyperperfusion and cognitive impairment after carotid endarterectomy: a diffusion tensor magnetic resonance imaging study[J]. Cerebrovasc Dis, 2012, 34(5-6): 358-367.
[DOI]
|
| [10] |
CHEN YR, TYMOFIYEVA O, HESS CP, et al. Effects of rejecting diffusion directions on tensor-derived parameters[J]. Neuroimage, 2015, 109: 160-170.
[DOI]
|
| [11] |
BOSHES B, PRIEST WS, YACORZYNSKI GK, et al. The neurologic, psychiatric and psychologic aspects of cardiac surgery[J]. Med Clin North Am, 1957, 41(1): 155-169.
[DOI]
|
| [12] |
PLANEL E, RICHTER KEG, NOLAN CE, et al. Anesthesia leads to tau hyperphosphorylation through inhibition of phosphatase activity by hypothermia[J]. J Neurosci, 2007, 27(12): 3090-3097.
[DOI]
|
| [13] |
BROWNDYKE JN, BERGER M, HARSHBARGER TB, et al. Resting-state functional connectivity and cognition after major cardiac surgery in older adults without preoperative cognitive impairment: preliminary findings[J]. J Am Geriatr Soc, 2017, 65(1): e6-e12.
|
| [14] |
MARTINS R, JOANETTE Y, MONCHI O. The implications of age-related neurofunctional compensatory mechanisms in executive function and language processing including the new temporal hypothesis for compensation[J]. Front Hum Neurosci, 2015, 9: 221.
|
| [15] |
HSHIEH TT, DAI WY, CAVALLARI MI, et al. Cerebral blood flow MRI in the nondemented elderly is not predictive of post-operative delirium but is correlated with cognitive performance[J]. J Cereb Blood Flow Metab, 2017, 37(4): 1386-1397.
[DOI]
|
| [16] |
ALSOP DC, DETRE JA, GROSSMAN M. Assessment of cerebral blood flow in Alzheimer's disease by spin-labeled magnetic resonance imaging[J]. Ann Neurol, 2000, 47(1): 93-100.
[DOI]
|
| [17] |
JOHNSON NA, JAHNG GH, WEINER MW, et al. Pattern of cerebral hypoperfusion in Alzheimer disease and mild cognitive impairment measured with arterial spin-labeling MR imaging: initial experience[J]. Radiology, 2005, 234(3): 851-859.
[DOI]
|
| [18] |
DAI WY, LOPEZ OL, CARMICHAEL OT, et al. Mild cognitive impairment and alzheimer disease: patterns of altered cerebral blood flow at MR imaging[J]. Radiology, 2009, 250(3): 856-866.
[DOI]
|
| [19] |
SCHEFF SW, PRICE DA, ANSARI MA, et al. Synaptic change in the posterior cingulate gyrus in the progression of Alzheimer's disease[J]. J Alzheimers Dis, 2015, 43(3): 1073-1090.
|
| [20] |
YOSHIDA T, KAZUI H, TOKUNAGA H, et al. Protein synthesis in the posterior cingulate cortex in Alzheimer's disease[J]. Psychogeriatrics, 2011, 11(1): 40-45.
[DOI]
|
| [21] |
XEKARDAKI A, RODRIGUEZ C, MONTANDON ML, et al. Arterial spin labeling may contribute to the prediction of cognitive deterioration in healthy elderly individuals[J]. Radiology, 2015, 274(2): 490-499.
[DOI]
|
| [22] |
BENTON AL, VVARNEY NR, HAMSHER KD. Visuospatial judgment.A clinical test[J]. Arch Neurol, 1978, 35(6): 364-367.
[DOI]
|
 2022, Vol. 49
2022, Vol. 49


