2. 复旦大学附属中山医院病理科 上海 200032;
3. 复旦大学附属上海市第五人民医院病理科 上海 201100
2. Department of Pathology, Zhongshan Hospital, Fudan University, Shanghai 200032, China;
3. Department of Pathology, Shanghai Fifth People's Hospital, Fudan University, Shanghai 201100, China
胃癌(gastric carcinoma,GC)是消化系统恶性肿瘤[1]。尽管治疗方面有进展,并且其发病率有所下降[2],但在中国恶性肿瘤总体发病率和死亡率排行中,它均居于第二位[3],5年生存率约为20%。胃癌的高死亡率除了与发病症状隐匿有关外,主要归因于晚期病例的高复发率和远处转移[4]。有研究显示,癌组织的浸润与转移是胃癌复发的重要临床指征,胃癌浸润与转移情况及患者预后紧密相关[5-6]。因此,胃癌进展的潜在机制研究十分重要。
黏着斑蛋白Vinculin是细胞黏附的主要调节剂[7],可将含肌动蛋白的微丝锚定在质膜上,并使细胞附着在基质上。自从Vinculin被鉴定以来,已经取得很多研究进展,其功能被逐渐了解。Vinculin结构保守,可参与多种化学信号转导过程。对其在细胞黏附、收缩变形、细胞迁移中的作用的研究发现,Vinculin对于传递机械力和协调机械信号事件非常重要。肿瘤转移需要细胞侵袭结缔组织,这实质上是一种机械作用,涉及黏附、形状改变、运动和力产生。而解除对Vinculin的调控,则会导致细胞黏附、收缩、运动和生长的改变[8],提示Vinculin可能影响着肿瘤的发生、转移和侵袭。
有报道认为,Vinculin在肺癌组织中的蛋白水平显著少于癌旁,且Vinculin表达与TNM分期以及淋巴结转移紧密相关[9]。在不同肿瘤中,Vinculin的蛋白水平并不一致。有报道发现Vinculin在前列腺癌、胰腺癌、肾癌等肿瘤中表达升高[10-12],而在鳞状细胞癌、神经内分泌瘤、结直肠癌等肿瘤中表达降低[13-14]。这些不一致的研究结果可能与实验所用的不同细胞有关,也可能因为Vinculin在不同类型的癌中有不同的表达特点。Vinculin是癌症的增强还是抑制因子目前尚无定论。
Vinculin在胃癌侵袭和转移中的生物学作用的研究较少。因此,我们拟检测Vinculin蛋白在临床样本中的表达情况。前期收集了110位患者的胃癌标本,结合随访信息等临床资料,使用免疫组织化学技术进行了检测,并统计分析Vinculin在标本中的表达量及其与主要临床指征(包括但不限于:肿瘤大小、分期、淋巴结转移、预后等)的相关性,通过对Vinculin蛋白水平的监测,为胃癌临床诊疗提供帮助。
材料和方法病理资料 应用同位素标记相对与绝对定量蛋白组学(isobaric tags for relative and absolute quantification,iTRAQ)技术检测的组织样本6例,为2009年5月—2010年6月在复旦大学附属肿瘤医院行手术切除全胃5例和近端胃1例标本。手术标本离体半小时内,在不影响后续诊疗的前提下切取小块肿瘤组织或距离肿瘤组织边缘10 cm以上的正常黏膜组织,立即低温冷冻保存;经病理证实,均为低分化腺癌(T4N2~3M0,Ⅲc),术后均行常规方案辅助化疗,依据2年内是否发生复发或远处转移,将病例分为复发组(无疾病进展时间3~14个月)3例与未复发组3例,以复发组远离瘤巢区正常黏膜组织为正常对照组。收集1990年2月—1998年7月110例胃腺癌根治术患者的临床病理资料。患者术前均未接受放、化疗。入院患者均签署了标本研究的知情同意书。所有病例均经两名资深病理医师再次复片确诊胃腺癌。收集的临床病理资料包括:患者年龄、性别、肿瘤部位及肿瘤大小、分化情况、脉管及神经束侵犯和淋巴结转移等。pTNM分期依据第8版美国癌症联合委员会(American Joint Committee on Cancer,AJCC)pTNM分期标准。
新鲜组织标本iTRAQ蛋白质谱检测 根据既往文献报道和操作规范[15]。(1)提取并标记组织蛋白,丙酮沉淀样品蛋白,还原剂还原样品蛋白,半胱氨酸封闭样品蛋白,用trypsin酶解蛋白样品;iTRAQ试剂分别标记样品酶解物——118标记复发组、119标记未复发组和121标记正常黏膜组,充分混合混匀。(2)第一维强阳离子交换(strong cation exchange,SCX)层析法分馏样品,添加缓冲液A,震荡混匀;以20 AD HPLC系统的SCX层析法分馏蛋白多肽,样品混合液添加到聚亚硫乙基柱(2.1 mm×100 mm,5 μm,200 Å),通过含有梯度为0、5%、10%、20%、40%、80%缓冲液B的缓冲液A,以200 μL/min的流速分离蛋白多肽60 min,检测样品在214 nm和280 nm的吸光度值(D),共搜集得到25个SCX馏分。缓冲液A:10 mmol/L KH2PO4,25%乙腈,pH=2.6;缓冲液B:10 mmol/L KH2PO4,5%乙腈,1 mol/L KCl,pH=2.6;Diluent:25% acetonitrile,pH=2.6。(3)第二维反相液质联用RPLC-MS/MS,上一级搜集到的馏分溶液,4 ℃下20 000×g真空离心风干30 min,复溶于50 μL HPLC缓冲液A,上样入ZORBAX 300SB-C18反相柱(5 μm,300 Å,0.1 mm×150 mm),以0.3 μL/min的流速通过5%~80%梯度的HPLC缓冲液B(95% ACN,0.1%蚁酸)90 min,通过联合20AD HPLC系统的QSTAR XL方法分析流通数据,由一级质谱(m/z:400~1 800)联合二级质谱(m/z:100~2 000),获得扫描数据。其中根据一级质谱(MS)的图像,选择4个峰值最高的片段,即前驱离子(precursors),进行二级扫描,获得串联二级质谱(MS/MS)的信息。每个SCX馏分进行串联分析/重复鉴定2次。MS数据通过ProteinPilot软件(v 4.2)在International Protein Index(IPI)数据库(v 3.45)中检索并鉴定多肽。(4)质谱校正并设定相应的参数。(5)由Paragon Algorithm检索多肽信息,确定候选蛋白,并经由软件自带的Pro Group Algorithm运算法则作进一步的验证。(6)差异蛋白的筛选:在前述候选蛋白的基础上,符合以下标准的蛋白质被认为有组间差异变化,用于进一步的分析研究,即①Unused ProtSore>1.3,至少1条肽链具有95%CI;②蛋白相对表达量阈值设为≥1.25或≤0.8;③P < 0.05。
石蜡包埋组织免疫组织化学染色 采用免疫组化增强标记聚合物系统(Enhance Labelled Polymer System,ELPS)法检测110例胃癌标本中Vinculin的表达。具体操作步骤严格遵照试剂盒说明书进行,组织切片常规脱蜡、水化,PBS缓冲液冲洗,一、二抗孵育,DAB显色,苏木精衬染及乙醇脱水干燥,中性树胶封固。一抗Vinculin抗体购自德国Sigma公司,鼠抗,1∶200;HRP偶联二抗、DAB均购自丹麦Dako公司。Vinculin表达定位在细胞胞质,阳性对照为平滑肌组织,阴性对照为淋巴细胞。分别评估染色的强度(staining intensity,SI)和阳性细胞百分率(positive proportion,PP),SI由无着色、浅黄色、棕黄色、黄褐色分别记为0~3分,PP由5%、25%、50%、75%截断值分别记为0~4分,免疫反应积分(immunoreactive score,IRS)=SI×PP,得分≥3分者判为阳性;得分 < 3分者判为阴性。
随访 患者均通过电话或者复查随访。无病生存期(disease free survival,DFS)指从患者手术之日起到出现复发、转移、死于食管癌的时间或死亡患者记录最后一次随访的时间。总生存期(overall survival,OS)定义为手术后到患者死亡的时间或最后1次随访的时间。随访截至2000年1月。
统计学分析 使用GraphPad Prism 6软件进行统计分析,以Spearman’s correlation和Pearson Chi-Square检验来检测Vinculin蛋白表达水平与主要临床病理指征之间的关联。由Kaplan-Meier生存曲线分析Vinculin蛋白表达水平与总体生存期的联系。P < 0.05为差异有统计学意义。
结果iTRAQ技术临床标本蛋白质谱检测结果 iTRAQ技术联合二维液相色谱串联质谱(2D LC-MS/MS),符合数据质量控制要求,按照95%的置信区间下Protein-Threshold>1.3的标准,鉴别出3 566条多肽,归纳识别出570种蛋白质。结合iTRAQ技术中ParagonTM Algorithm运算法则的结果和文献参考,筛选具有组间差异性表达的蛋白,胃癌复发组相对于正常胃黏膜组差异表达的蛋白有13种,其中2种(Keratin/type Ⅰ cytoskeletal 19、Matrin-3)表达上升、11种(Neuroblast differentiation-associated protein AHNAK、Filamin-A、Hemoglobin subunit、Vinculin、ATP synthase subunit alpha,mitochondrial等)表达下降;胃癌未复发组相对于正常胃黏膜组差异表达的蛋白有8种,其中5种表达上升、3种表达下降,但多数差异无统计学意义。其中,相对正常黏膜组,Vinculin蛋白在胃癌复发组表达水平降低(118:121倍值为0.787,P=0.004),而在胃癌非复发组的表达差异无统计学意义(P=0.058)。
胃癌临床标本中Vinculin蛋白质的表达情况
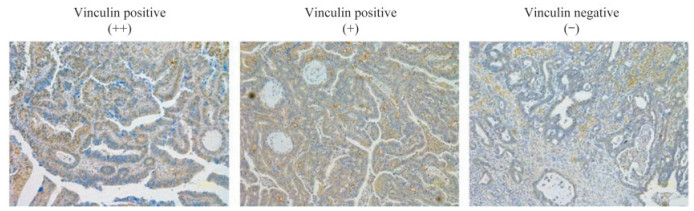
在110例人胃癌组织标本中,Vinculin阳性46例(41.8%)、阴性64例(58.2%)(图 1)。
|
| 图 1 胃癌组织中Vinculin表达的代表性IHC染色结果(200×) Fig 1 Representative IHC staining of Vinculin expression in GC tissue (200×) |
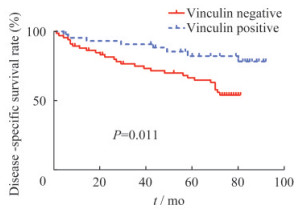
胃癌石蜡组织标本中Vinculin蛋白质的表达与总生存率的相关性 具有完整随访资料86例,随访1~92个月,患者1、3、5年总体生存率分别为88.4%、77.9%和69.7%;Vinculin阳性和阴性患者的中位总生存期(overall survival,OS)分别为36个月和28个月。Kaplan-Meier生存分析显示,Vinculin阴性患者的总生存率低于Vinculin阳性患者(P=0.011,图 2)。
|
| 图 2 Vinculin阳性与阴性患者总体生存率分析 Fig 2 Kaplan-Meier survival analysis of GC grouped by positive or negative expression of Vinculin |
胃癌临床标本中Vinculin蛋白质的表达与临床病理特征的关系 统计结果显示,Vinculin的低表达与淋巴结转移(P=0.018)、肿瘤TNM分期(P=0.022)、血管侵袭(P=0.002)具有显著的相关性(表 1、表 2)。
| Characteristics | Number of patients/Total Number (%) |
| Age (y) | |
| Median (range) | 68.4 (42-81) |
| Gender | |
| Male | 67 (60.9) |
| Female | 43 (39.1) |
| Tumor size (cm) | |
| < 4 | 60 (54.5) |
| ≥4 | 50 (45.5) |
| Tumor location | |
| Upper | 8 (7.3) |
| Middle | 19 (17.3) |
| Lower | 83 (75.4) |
| Invasion depth | |
| T1 | 68 (61.8) |
| T2 | 26 (23.6) |
| T3 | 16 (14.6) |
| Lymph node metastasis | |
| N0 | 56 (50.9) |
| N1 | 12 (10.9) |
| N2 | 11 (10.0) |
| N3 | 31 (28.2) |
| Distant metastasis | |
| M0 | 93 (84.5) |
| M1 | 17 (15.5) |
| TNM classification | |
| Ⅰ | 51 (46.4) |
| Ⅱ | 22 (20.0) |
| Ⅲ | 20 (18.2) |
| Ⅳ | 17 (15.4) |
| Vascular invasion | |
| Yes | 44 (40.0) |
| No | 66 (60.0) |
| Survival status | |
| Alive | 50/86 (58.1) |
| Dead | 36/86 (41.9) |
| TNM:Tumor lymph-node metastasis. | |
| [n(%)] | |||||||||||||||||||||||||||||
| Characteristics | Expression | P | χ2 | ||||||||||||||||||||||||||
| Positive | Negative | ||||||||||||||||||||||||||||
| All cases | 46 (41.8) | 64 (58.2) | |||||||||||||||||||||||||||
| Age (y) | 0.332 | 1.546 | |||||||||||||||||||||||||||
| < 65 | 18 (36.7) | 31 (63.3) | |||||||||||||||||||||||||||
| ≥65 | 28 (45.9) | 33 (54.1) | |||||||||||||||||||||||||||
| Gender | 0.001 | 10.089 | |||||||||||||||||||||||||||
| Male | 20 (29.9) | 47 (70.1) | |||||||||||||||||||||||||||
| Female | 26 (60.5) | 17 (39.5) | |||||||||||||||||||||||||||
| Tumor size (cm) | 0.129 | 2.303 | |||||||||||||||||||||||||||
| < 4 | 29 (44.7) | 31 (55.3) | |||||||||||||||||||||||||||
| ≥4 | 17 (78.6) | 33 (21.4) | |||||||||||||||||||||||||||
| Tumor location | 0.501 | 1.383 | |||||||||||||||||||||||||||
| Upper | 2 (25.0) | 6 (75.0) | |||||||||||||||||||||||||||
| Middle | 7 (36.8) | 12 (63.2) | |||||||||||||||||||||||||||
| Lower | 37 (44.6) | 46 (55.4) | |||||||||||||||||||||||||||
| Invasion depth | 0.331 | 2.209 | |||||||||||||||||||||||||||
| T1 | 30 (44.1) | 38 (55.9) | |||||||||||||||||||||||||||
| T2 | 12 (46.2) | 14 (53.8) | |||||||||||||||||||||||||||
| T3 | 4 (25.0) | 12 (75.0) | |||||||||||||||||||||||||||
| Lymph node metastasis | 0.018 | 10.073 | |||||||||||||||||||||||||||
| N0 | 30 (53.6) | 26 (46.4) | |||||||||||||||||||||||||||
| N1 | 6 (50.0) | 6 (50.0) | |||||||||||||||||||||||||||
| N2 | 4 (36.4) | 7 (63.6) | |||||||||||||||||||||||||||
| N3 | 6 (19.4) | 25 (80.6) | |||||||||||||||||||||||||||
| Distant metastasis | 0.041 | 3.157 | |||||||||||||||||||||||||||
| M0 | 41 (44.1) | 52 (55.9) | |||||||||||||||||||||||||||
| M1 | 3 (17.6) | 14 (82.4) | |||||||||||||||||||||||||||
| TNM classification | 0.022 | 9.632 | |||||||||||||||||||||||||||
| Ⅰ | 26 (51.0) | 25 (49.0) | |||||||||||||||||||||||||||
| Ⅱ | 12 (54.5) | 10 (45.5) | |||||||||||||||||||||||||||
| Ⅲ | 5 (25.0) | 15 (75.0) | |||||||||||||||||||||||||||
| Ⅳ | 3 (17.7) | 14 (82.3) | |||||||||||||||||||||||||||
| Vascular invasion | 0.002 | 9.116 | |||||||||||||||||||||||||||
| Yes | 10 (46.9) | 34 (53.1) | |||||||||||||||||||||||||||
| No | 34 (51.5) | 32 (48.5) | |||||||||||||||||||||||||||
| Survival status | 0.004 | 7.764 | |||||||||||||||||||||||||||
| Alive | 26 (51.4) | 24 (48.6) | |||||||||||||||||||||||||||
| Dead | 8 (22.2) | 28 (77.8) | |||||||||||||||||||||||||||
| TNM:Tumor lymph-node metastasis. | |||||||||||||||||||||||||||||
Vinculin是在黏着斑中发现的一种分布于胞质的蛋白,参与细胞外基质(extracellular matrix,ECM)与肌动蛋白细胞骨架的连接过程。近些年,Vinculin的下调陆续在几个高度转移性癌细胞中被发现[13, 16-18]。但是目前尚未发现对Vinculin在胃癌中表达的报道,Vinculin对胃癌侵袭和转移的作用以及对胃癌复发的影响尚不明确。
本课题运用iTRAQ技术在临床胃癌复发组、未复发组和正常胃黏膜组进行蛋白质质谱扫描。在鉴别出的570种蛋白中,挑选出有组间差异表达的蛋白质,与正常胃黏膜组相比,黏着斑蛋白Vinculin在胃癌复发组表达显著下调,而在胃癌未复发组表达差异不显著。提示Vinculin蛋白可能在胃癌的复发中具有一定的功能和影响,但其在胃癌侵袭和转移中的生物学作用还有待进一步探索。
为进一步分析筛选出的差异表达蛋白质的功能聚类,我们对差异蛋白作GO(Gene Ontology)分析。运用Gene Ontology-AmiGO 2提供的在线分析工具PANTHER Classification System,对差异蛋白做功能聚类分析:发现蛋白分子功能集中在结合肌动蛋白、酶催化活性调节、细胞结构分子活性等;主要参与到细胞黏附、细胞骨架结构重排、代谢过程等生物学进程。
接着对这些蛋白作KEGG(京都基因与基因组百科全书) Pathway分析。KEGG是基因组破译方面的数据库,使用计算机技术利用基因信息对更高层次和更复杂细胞活动和生物体行为作出计算推测。可能由于筛选出的蛋白量较少,未能得到Pathway的聚簇。
在110例石蜡包埋的胃癌临床标本组织中,我们采用免疫组织化学技术,检测了Vinculin的蛋白表达水平,并根据免疫组化结果,分析了Vinculin与临床病理参数以及患者生存率的关系。根据免疫组织化学染色评分结果,我们发现,Vinculin的缺失表达与胃癌淋巴结转移、肿瘤TNM分期、血管侵袭均具有显著的相关性,提示胃癌恶性程度越高,Vinculin表达越低。生存曲线分析结果提示,Vinculin缺失表达与胃癌患者较短的生存期有关联,提示Vinculin蛋白是胃癌患者生存预后具有意义的分子指标。
细胞-细胞黏附的丧失对于癌症侵袭和转移的发展是重要的[18],既往研究[19]显示,黏着斑蛋白缺损与细胞黏附减少和细胞运动增加有关,表明其可能在转移性生长中起作用。Yang等[20]在结直肠癌中发现黏着斑蛋白表达下降与肿瘤发生和转移风险增加之间存在关联。本研究结果显示,Vinculin缺失表达与胃癌的侵袭和转移正相关,Vinculin表达减少,将会使胃癌细胞黏附减少,运动性增加,导致癌细胞的分离和向基底膜的侵袭。
我们通过iTRAQ蛋白质谱分析,发现Vinculin在胃癌复发相关因素中具有差异性表达;在临床标本验证中发现Vinculin的缺失表达与胃癌的侵袭转移显著正相关,通过临床胃癌组织标本的检测,我们初步确认了Vinculin蛋白的缺失表达与胃癌肿瘤的发生发展具有显著相关性,并提示患者预后不良。但目前研究样本量较少,也受到诸如临床标本选择、样本类型和数量等因素的影响,其内在机制尚待进一步探究。在以后的研究中,可增加样本量,并深入探究Vinculin表达水平对胃癌细胞的生物学行为(增殖能力、克隆形成能力、体外侵袭转移能力等)的影响及其发挥生物学作用的相关分子机制。
我们的研究表明,Vinculin的低表达与胃癌的淋巴结转移、肿瘤TNM分期、血管侵袭显著正相关。Vinculin表达情况或可作为胃癌患者生存的预测因子。
作者贡献声明 卢珊 文献调研与整理,论文撰写和修改。张磊 论文构思与修改,数据采集,实验实施。苏莹,侯陈建,王美丽 论文修订。刘秀萍 监督指导。
利益冲突声明 所有作者均声明不存在利益冲突。
| [1] |
LOGAN RP. Helicobacter pylori and gastric cancer[J]. Lancet, 2019, 344(8929): 1078-1079.
|
| [2] |
FORMAN D, KINLEN L. Declining incidence of gastric cancer[J]. BMJ, 2019, 303(6796): 248-249.
|
| [3] |
SIEGEL RL, MILLER KD, JEMAL A. Cancer Statistics, 2017[J]. CA Cancer J Clin, 2017, 67(1): 7-30.
[DOI]
|
| [4] |
VAN CUTSEM E, SAGAERT X, TOPAL B, et al. Gastric cancer[J]. Lancet, 2016, 388(10060): 2654-2664.
[DOI]
|
| [5] |
张学伟, 郑安斌, 石炜, 等. 胃癌根治术后复发转移的影响因素及其对预后的影响[J]. 实用癌症杂志, 2015, 30(7): 1062-1064. [DOI]
|
| [6] |
LU J, WANG YH, YOON C, et al. Circular RNA circ-RanGAP1 regulates VEGFA expression by targeting miR-877-3p to facilitate gastric cancer invasion and metastasis[J]. Cancer Lett, 2020, 471: 38-48.
[DOI]
|
| [7] |
IZARD T, BROWN DT. Mechanisms and functions of vinculin interactions with phospholipids at cell adhesion sites[J]. J Biol Chem, 2016, 291(6): 2548-2555.
[DOI]
|
| [8] |
GOLDMANN WH, AUERNHEIMER V, THIEVESSEN I, et al. Vinculin, cell mechanics and tumour cell invasion[J]. Cell Biol Int, 2013, 37(5): 397-405.
[DOI]
|
| [9] |
YU Q, XU L, CHEN L, et al. Vinculin expression in non-small cell lung cancer[J]. J Int Med Res, 2020, 48(1): 1-9.
|
| [10] |
WANG Y, KURAMITSU Y, UENO T, et al. Proteomic differential display identifies upregulated vinculin as a possible biomarker of pancreatic cancer[J]. Oncol Rep, 2012, 28(5): 1845-1850.
[DOI]
|
| [11] |
KAWAKAMI K, FUJITA Y, KATO T, et al. Integrin β4 and vinculin contained in exosomes are potential markers for progression of prostate cancer associated with taxane-resistance[J]. Int J Oncol, 2015, 47(1): 384-390.
[DOI]
|
| [12] |
SHI X, GUO X, LI X, et al. Loss of Linc01060 induces pancreatic cancer progression through vinculin-mediated focal adhesion turnover[J]. Cancer Lett, 2018, 433: 76-85.
[DOI]
|
| [13] |
LI T, GUO H, SONG Y, et al. Loss of vinculin and membrane-bound β-catenin promotes metastasis and predicts poor prognosis in colorectal cancer[J]. Mol Cancer, 2014, 13: 263.
[DOI]
|
| [14] |
LIU M, OBERG K, ZHOU Y. Expression and function of vinculin in neuroendocrine tumors[J]. Tumour Biol, 2007, 28(4): 196-204.
[DOI]
|
| [15] |
UNWIN RD, GRIFFITHS JR, WHETTON AD. Simultaneous analysis of relative protein expression levels across multiple samples using iTRAQ isobaric tags with 2D nano LC-MS/MS[J]. Nat Protoc, 2010, 5(9): 1574-1582.
[DOI]
|
| [16] |
TOMA-JONIK A, WIDLAK W, KORFANTY J, et al. Active heat shock transcription factor 1 supports migration of the melanoma cells via vinculin down-regulation[J]. Cell Signal, 2015, 27(2): 394-401.
[DOI]
|
| [17] |
GAO Y, WANG Z, HAO Q, et al. Loss of ERα induces amoeboid-like migration of breast cancer cells by downregulating vinculin[J]. Nat Commun, 2017, 8: 14483.
[DOI]
|
| [18] |
VILLENEUVE C, LAGOUTTE E, PLATER LD, et al. aPKCi triggers basal extrusion of luminal mammary epithelial cells by tuning contractility and vinculin localization at cell junctions[J]. PNAS, 2019, 116(48): 201906779.
|
| [19] |
RODRÍGUEZ FERNÁNDEZ JL, GEIGER B, SALOMON D, et al. Suppression of vinculin expression by antisense transfection confers changes in cell morphology, motility, and anchorage-dependent growth of 3T3 cells[J]. J Cell Biol, 1993, 122(6): 1285-1294.
[DOI]
|
| [20] |
YANG HJ, CHEN JZ, ZHANG WL, et al. Focal adhesion plaque associated cytoskeletons are involved in the invasion and metastasis of human colorectal carcinoma[J]. Cancer Invest, 2010, 28(2): 127-134.
|
 2022, Vol. 49
2022, Vol. 49


