2. 上海市浦东新区疾病预防控制中心 上海 200136;
3. 复旦大学浦东预防医学研究院 上海 200136
2. Center for Disease Control and Prevention of Pudong New Area, Shanghai 200136, China;
3. Pudong Preventive Medicine Research Institute, Fudan University, Shanghai 200136, China
慢性阻塞性肺病(chronic obstructive pulmonary disease,COPD)是一种常见的慢性疾病,以气道阻塞为主要特征[1]。据估计,截至2015年我国COPD患者高达9 900万人,人群总患病率约8.6%,40岁以上社区人群中COPD患病率达13.7%[2]。此外,全球疾病负担(global burden of disease,GBD)数据表明,1990年至2017年,COPD一直是我国位列前三的主要死因[3]。除了较高的患病率以及死亡率,COPD还带来沉重的社会经济负担[4-5],是我国重要的公共卫生问题。
COPD进程难以逆转,其治疗和看护以缓解症状为主,旨在改善患者的生命质量[6]。患者生命质量及其影响因素成为COPD研究中的重要内容。COPD患者的生命质量受诸多因素的影响,包括呼吸道症状[7]、心理因素[8]、合并症[9]等,睡眠问题在COPD患者中亦非常普遍[10]。尽管研究提示患者的睡眠问题与生命质量存在一定的关联,但是此类研究多纳入病情较为严重的患者[7],这些患者更易受到COPD相关症状和体征影响而发生睡眠紊乱[11-12]。少有研究关注轻中度及稳定期的COPD患者[13],尤其是社区轻中度COPD患者。因此,本研究拟采用横断面研究,综合评价社区轻中度COPD患者的睡眠质量与生命质量之间的关联。
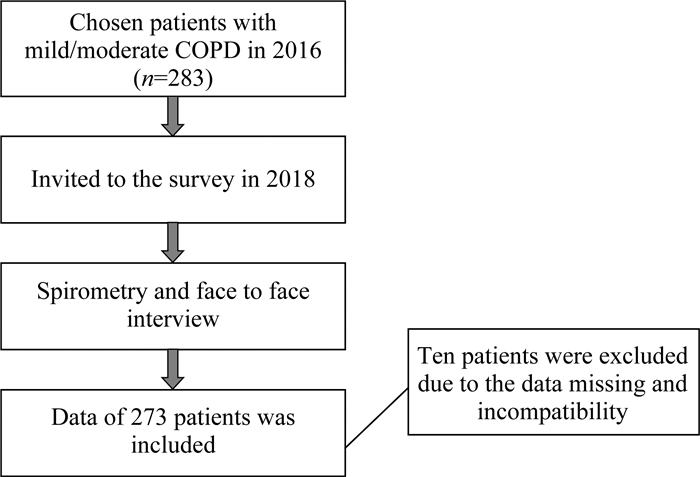
资料和方法研究对象及研究设计 本研究为横断面研究,以上海市浦东新区既往开展的COPD调查中的283名来自社区的轻中度COPD患者为研究对象[14]。研究对象来自通过整群随机抽样选取的6个社区,于2018年12月开展现场调查,并将其中符合标准的COPD患者纳入分析。纳入标准:(1)经由二、三级医院临床医师诊断为COPD并纳入浦东新区COPD管理;(2)基线调查肺功能检测提示仍处于轻度或中度COPD;(3)年龄在40岁以上;(4)上海市户籍居民或居住≥6个月的常住人口;(5)自愿且有能力签署知情同意书并提供医疗记录。排除标准:(1)身体处于严重或不稳定的状态,如心血管疾病、神经性疾病、骨骼肌肉损伤或近一个月内发生过COPD急性加重;(2)具有认知障碍或运动受限。最终273位患者纳入本次研究,合格率为96.46%(图 1)。本研究经浦东新区疾病预防控制中心医学伦理委员会批准,所有患者全部签署知情同意书。
|
| 图 1 研究对象入选流程图 Fig 1 Flow chart of participants' enrollment |
睡眠质量评价 研究对象的睡眠质量评价采用中文版匹兹堡睡眠质量指数量表(Pittsburgh Sleep Quality Index,PSQI)。该量表已经过信效度检验[15],包含19个问题,从以下7个不同的维度评价睡眠质量:(1)自我感知睡眠质量;(2)入睡时间;(3)睡眠时长;(4)睡眠效率;(5)睡眠障碍;(6)睡眠药物的使用;(7)日间功能障碍。每个维度得分合计0~3分,PSQI总分为0~21分。将所有患者分为两组:睡眠质量较好组(PSQI≤7)与睡眠质量较差组(PSQI > 7)。此外,本研究还采用一种被验证的三因子模型作为对不同睡眠维度的探讨[16],(1)睡眠效率因子:由睡眠时长以及睡眠效率两个维度组成,总分为0~6;(2)睡眠质量:由自我感知睡眠质量、入睡时间及睡眠药物的使用三个维度组成,总分为0~9;(3)日常睡眠紊乱:由睡眠障碍及日间功能障碍两个维度组成,总分为0~6。
生命质量评价 患者的生命质量通过中文版欧洲五维三水平量表(EQ-5D-3L)进行评价,包括5个维度:行动能力、自己照顾自己能力、日常活动能力、疼痛或不舒服及焦虑或抑郁。每个维度又包含3个水平,即没有任何困难(1分)、有些困难(2分)和有极度困难(3分),根据5个维度的得分可以得到243种健康状态组合,其中“11111”代表健康状态最佳,“33333”代表健康状态最差。采用中国人群偏好的时间权衡法对其转换后得到相应的健康效应值范围为-0.149~1,1代表健康完全没有问题,-0.149说明健康处于最差的状态[17]。
人群基本特征 采用框架式调查问卷获取患者相关信息,包括一般人口学特征、病程、其他慢性疾病情况(哮喘,心脏疾病)、COPD药物使用、吸烟史、二手烟接触、规律性身体活动等。
数据录入与统计学分析 患者生命质量以EQ-5D-3L量表计算所得的健康效应值作为因变量,将其根据效应值是否为1进行分组后,采用Logistic回归分析,评价不同睡眠质量对生命质量的比值比。回归方程校正年龄、性别、BMI、体育锻炼情况、二手烟接触、COPD病程、急性加重发生、COPD药物使用、是否患有哮喘等因素。
所有数据通过Epidata 3.1双份录入核查,数据分析使用SPSSS 22.0软件。P < 0.05为差异有统计学意义。
结果人群基本特征 共有273名患者完成调查并纳入分析,应答率为100%。轻度COPD患者占96.7%(264/273),60岁以上患者占79.1%(216/273)。在过去一年间有27.5%(75/273)的患者发生过急性加重,13.9%(38/273)的患者同时患有心脏相关疾病,接近一半的患者(127/273,47.7%)在COPD稳定期间不使用相关药物(表 1)。
| Variables | Cases [n (%)] |
| Age (y) | |
| < 60 | 57 (20.9) |
| ≥60 | 216 (79.1) |
| Gendera | |
| Male | 132(48.4) |
| Female | 141(51.6) |
| BMI a(kg/m2) | |
| < 25 | 146 (53.5) |
| ≥25 | 124 (46.5) |
| Level of education (y) | |
| ≤9 | 226(82.8) |
| > 9 | 47(17.2) |
| Physical activity(> 30 min) | |
| < once per week | 133(48.7) |
| ≥ once per week | 140(51.3) |
| Smokingb | |
| Never | 160(58.8) |
| Ex/current smokers | 112(41.2) |
| Passive smoking(over 15 min per week)c | |
| No | 87(32.0) |
| Yes | 185(68.0) |
| Severity of COPD | |
| Mild | 264(96.7) |
| Moderate | 9(3.3) |
| Duration of COPD (y) | |
| < 10 | 194(71.1) |
| ≥10 | 79(28.9) |
| Exacerbation during last year | |
| No | 198(72.5) |
| Yes | 75(27.5) |
| Inhaler for COPD | |
| No | 131(48.0) |
| Yes | 142(52.0) |
| Self-reported asthma | |
| No | 231(84.6) |
| Yes | 42(15.4) |
| Self-reported cardiovascular diseases | |
| No | 235(86.1) |
| Yes | 38(13.9) |
| Self-reported complications | |
| No | 264(96.7) |
| Yes | 9(3.3) |
| Mental status (HADS) | |
| Anxiety (positive) | 10(3.7) |
| Depression (positive) | 19(7.0) |
| a3 cases missing;b1 case missing;c1 case missing. | |
生命质量及睡眠的基本情况 社区轻中度COPD患者的EQ-5D-3L效应值平均得分为0.938±0.094。最常见的问题为疼痛与不适,约27.1%(74/273)的患者报告中度及以上的疼痛与不适,其次是焦虑抑郁(13.6%,37/273)。最常见的健康状态为11111,占64.5%(176/273)。PSQI的结果表明,患者的中位得分为5.50(3.00,9.00),29.3%(80/274)患者的睡眠状况较差(PSQI > 7),睡眠效率、睡眠质量及日常睡眠障碍的中位得分分别为1.00(0.00,3.00)、2.00(0.00,3.00)和2.00(1.00,3.00)。
生命质量与睡眠质量之间的关联 采用EQ-5D-3L效应值等于1将生命质量得分分成较好与较差组别,进行多因素Logistic回归分析,在调整相关混杂因素之后,相比于睡眠质量较好的患者(PSQI≤7),睡眠质量较差的患者(PSQI > 7)生命质量较差的可能性更大(OR=1.80,95%CI:1.03~3.14)。在排除中度COPD患者之后,这一结果无显著变化,轻度COPD患者中相应OR值为1.90(95%CI:1.07~3.36)。具体见表 2。
| Variable Poor sleepers vs. Good sleepers (PSQI≤7 vs. PSQI > 7) |
Utility (All patients) | Utility (Patients with mild COPD) | |||
| ORad (95%CI) | P | ORad (95%CI) | P | ||
| Univariate analysis | 1.77(1.04-3.02) | 0.036 | 1.90 (1.10-3.29) | 0.022 | |
| Multivariate analysis | |||||
| Model 1 | 1.82(1.06-3.15) | 0.031 | 1.97 (1.12-3.45) | 0.018 | |
| Model 2 | 1.80(1.03-3.14) | 0.038 | 1.91 (1.08-3.37) | 0.027 | |
| Model 3 | 1.80(1.03-3.14) | 0.038 | 1.90 (1.07-3.36) | 0.028 | |
| Model 1:Adjusted age, gender, BMI, physical activities and smoking; Model 2:Adjusted duration of COPD, exacerbation, inhaler for COPD and all variables in model 1;Model 3:Adjusted self-reported asthma and all variables in model 2. | |||||
轻度COPD患者生命质量与不同睡眠因子之间的关联分析提示(表 3),日常睡眠紊乱与患者生命质量有关(OR=1.26,95%CI:1.02~1.56)。
| Variables | Utility (Logistic regression) | |
| ORad (95%CI) | P | |
| Factor 1:Sleep efficiency/ 1 point | 1.06(0.92-1.24) | 0.299 |
| Factor 2:Sleep quality/ 1 point | 1.06(0.91-1.23) | 0.282 |
| Factor 3:Daily disturbance/ 1 point | 1.26(1.02-1.56) | 0.029 |
| Model was adjusted by age, gender, BMI, physical activities and smoking, duration of COPD, exacerbation, inhaler for COPD and self-reported asthma. | ||
本研究通过对上海市浦东新区社区轻中度COPD患者的横断面调查发现,COPD患者的睡眠质量与生命质量之间存在关联,即睡眠较差的患者生命质量处于较差水平的可能性增加。
本研究结果提示,浦东新区社区轻中度COPD患者整体生命质量较好,生命质量效应值平均得分为0.934,低于中国一般人群生命质量的平均水平。据2013年国家卫生服务调查结果表明,中国人群的生命质量效应值平均得分为0.985[18]。然而,本文结果却远高于其他基于COPD患者的研究结果,周挺等[19]针对中国慢性非传染性疾病的系统综述发现,COPD患者的生命质量效应值在0.64~0.80[19]。这种差异可能由不同研究之间COPD患者严重程度的分布差异导致。本研究主要以轻度COPD患者为主,而吴敏敏等[20]的研究中,轻度患者仅占五分之一,超过三分之一的患者患有重度及极重度COPD,其研究结果表明在轻度患者中,疼痛和不舒服是最常见的健康问题,这与本研究中的结果一致。
COPD患者中睡眠质量较差是常见问题,通常受到失眠等睡眠问题或者夜间咳嗽、打鼾等呼吸道症状的影响[21]。本研究中睡眠质量较差(PSQI > 7)的患者比例约29.3%,低于其他研究结果[11, 22]。多因素Logistic回归的结果显示,睡眠质量较差的患者生命质量处于较低水平的风险更大,调整后的OR值为1.80,这与Akinci等[7]和Dignani等[23]的研究结论相类似。但不同的是,本研究所有的患者均为轻中度COPD患者,考虑到睡眠问题可能会引起患者免疫力降低[24]和认知功能下降[25],甚至会增加COPD患者急性加重的风险[26],睡眠质量对于轻中度患者也是极为重要的相关因素。进一步排除中度患者后,轻度COPD患者的睡眠质量与生命质量的关联并未有明显改变,提示轻度COPD患者中睡眠问题仍然是影响生命质量的重要因素。在轻度患者中,只有日常睡眠紊乱因子与生命质量有显著关系,提示轻度COPD患者的生命质量较低可能源于日常睡眠紊乱。
本研究中除单纯COPD患者外,约有15.4%的患者同时自报有哮喘,即可能存在哮喘慢阻肺重叠症。胡红等[27]在研究中指出,50岁以下患者哮喘慢阻肺重叠症发病率 < 10%,但80岁以上发病率高达50%,提示随着年龄增加,重叠症发病率上升,本研究中79.1%患者年龄在60岁以上,合并有哮喘的患者比例为15.4%,处于比较合理的情况。为了避免哮喘对结果的影响,在模型2的基础上增加了哮喘作为校正因子(模型3)。结果发现,相比于模型2,调整后的OR值无明显改变,因此认为哮喘对研究结果无明显影响。
一项中国开展的大规模人群调查的结果显示,COPD患者中超过半数为轻度(GOLD Ⅰ期),而仅有7.4%的COPD患者为重度(GOLD Ⅲ期)及极重度(GOLD Ⅳ期)[28]。较重的COPD患者更容易因症状而寻诊,轻中度患者可能寻诊不频繁,主要依靠社区管理或自我管理,可能对COPD的病情变化不甚敏感,因此需要针对社区轻中度患者进行调查和研究。本研究关注COPD患者的睡眠和生命质量。睡眠是人体必需的生理过程,其变化容易被患者察觉,生命质量是持续性的慢性非传染性疾病的重要指标,易于察觉的不良因素和易于调查的生命质量,可以在社区监控或自我管理中起到作用。
本研究也存在一定的局限性。首先,所采用的横断面研究设计无法判断睡眠质量与生命质量之间的因果关系。其次,自我评价式的量表存在一定的局限,EQ5D存在一定的天花板效应,尤其是EQ-5D-3L,使得轻微的健康状态改变难以被识别,可采用尺度更多的E1-5D-5L或其他生命质量量表来解决这个问题;而PSQI基于多种常见睡眠问题对睡眠质量进行描述,无法细致拆分特定的睡眠特征。如需调查某种睡眠特征,可能需要采用更加特化的定量量表,如针对阻塞性呼吸暂停的睡眠呼吸暂停初筛变(Stop-Bang)以及评价日间疲劳的Epworth嗜睡量表(Epworth Sleepiness Scale,ESS),或是使用仪器采集客观的睡眠。此外,受样本量局限,未能就心理、呼吸道相关症状等因素的影响予以分析。
综上所述,本研究对社区轻中度COPD患者的横断面调查提示,该群体的生命质量受到睡眠质量影响显著,睡眠质量较差的患者生命质量相对较低,在社区COPD防治策略中,应对此予以考虑,提升COPD患者疾病过程的生命质量。
作者贡献声明 徐芊 论文撰写和数据分析。阮晓楠 研究设计,论文审阅和调查监督。吴抗,杨屹,王莹莹 现场调查,数据录入和清洗。邱桦,刘晓琳,王小楠,柯居中,李智韬,陈晓丹,刘庆平,林涛 现场调查,数据收集和核查。付朝伟 研究设计。王娜 研究设计,论文审阅。
利益冲突声明 所有作者均声明不存在利益冲突。
| [1] |
GLOBAL INITIATIVE FOR CHRONIC OBSTRUC-TIVE LUNG DISEASE. Global strategy for the diagnosis, management, and prevention of chronic obstructive pulmonary disease[EB/OL]. (2020-06-25)[2020-11-25]. http://www.goldcopd.org/.
|
| [2] |
WANG C, XU J, YANG L, et al. Prevalence and risk factors of chronic obstructive pulmonary disease in China (the China Pulmonary Health[CPH] study): a national cross-sectional study[J]. Lancet, 2018, 391(10131): 1706-1717.
[DOI]
|
| [3] |
ZHOU M, WANG H, ZENG X, et al. Mortality, morbidity, and risk factors in China and its provinces, 1990-2017:a systematic analysis for the Global Burden of Disease Study 2017[J]. Lancet, 2019, 394(10204): 1145-1158.
[DOI]
|
| [4] |
毛鸿彦, 蔡乐, 舒占坤, 等. 云南省农村居民慢性阻塞性肺疾病患病率及经济负担[J]. 中国慢性病预防与控制, 2012, 20(3): 244-246. [CNKI]
|
| [5] |
李建, 冯芮华, 崔月颖, 等. 我国三级医院药物治疗慢阻肺患者的经济负担分析[J]. 中国卫生经济, 2015, 34(9): 66-68. [CNKI]
|
| [6] |
MONTEAGUDO M, RODRIGUEZ-BLANCO T, LLAGOSTERA M, et al. Factors associated with changes in quality of life of COPD patients: a prospective study in primary care[J]. Respir Med, 2013, 107(10): 1589-1597.
[DOI]
|
| [7] |
AKINCI B, ASLAN GK, KIYAN E. Sleep quality and quality of life in patients with moderate to very severe chronic obstructive pulmonary disease[J]. Clin Respir J, 2018, 12(4): 1739-1746.
[DOI]
|
| [8] |
BORDONI B, MARELLI F, MORABITO B, et al. Depression, anxiety and chronic pain in patients with chronic obstructive pulmonary disease: the influence of breath[J]. Monaldi Arch Chest Dis, 2017, 87(1): 811.
[PubMed]
|
| [9] |
BURGEL PR, ESCAMILLA R, PEREZ T, et al. Impact of comorbidities on COPD-specific health-related quality of life[J]. Respir Med, 2013, 107(2): 233-241.
[DOI]
|
| [10] |
TSAI SC. Chronic obstructive pulmonary disease and sleep related disorders[J]. Curr Opin Pulm Med, 2017, 23(2): 124-128.
[DOI]
|
| [11] |
SCHARF SM, MAIMON N, SIMON-TUVAL T, et al. Sleep quality predicts quality of life in chronic obstructive pulmonary disease[J]. Int J Chron Obstruct Pulmon Dis, 2010, 6: 1-12.
[URI]
|
| [12] |
BASILE M, BAIAMONTE P, MAZZUCA E, et al. Sleep disturbances in COPD are associated with heterogeneity of airway obstruction[J]. COPD, 2018, 15(4): 350-354.
[DOI]
|
| [13] |
VALIPOUR A, LAVIE P, LOTHALLER H, et al. Sleep profile and symptoms of sleep disorders in patients with stable mild to moderate chronic obstructive pulmonary disease[J]. Sleep Med, 2011, 12(4): 367-372.
[DOI]
|
| [14] |
XIAO T, ZHOU X, HE Y, et al. Pain problems for patients with mild and moderate chronic obstructive pulmonary disease-a community-based study in Shanghai[J]. J Pain Res, 2017, 10: 2247-2252.
[DOI]
|
| [15] |
刘贤臣, 唐茂芹. 匹兹堡睡眠质量指数的信度和效度研究[J]. 中华精神科杂志, 1996, 29(2): 103-107. [CNKI]
|
| [16] |
COLE JC, MOTIVALA SJ, BUYSSE DJ, et al. Validation of a 3-factor scoring model for the Pittsburgh sleep quality index in older adults[J]. Sleep, 2006, 29(1): 112-116.
[DOI]
|
| [17] |
LIU GG, WU HY, LI MH, et al. Chinese time trade-off values for EQ-5D health states[J]. Value Health, 2014, 17(5): 597-604.
[DOI]
|
| [18] |
YAO Q, LIU C, ZHANG Y, et al. Changes in health-related quality of life of Chinese populations measured by the EQ-5D-3L: a comparison of the 2008 and 2013 National Health Services Surveys[J]. Health Qual Life Outcomes, 2019, 17(1): 43.
[DOI]
|
| [19] |
ZHOU T, GUAN H, YAO J, et al. The quality of life in Chinese population with chronic non-communicable diseases according to EQ-5D-3L: a systematic review[J]. Qual Life Res, 2018, 27(11): 2799-2814.
[DOI]
|
| [20] |
WU M, ZHAO Q, CHEN Y, et al. Quality of life and its association with direct medical costs for COPD in urban China[J]. Health Qual Life Outcomes, 2015, 13: 57.
[DOI]
|
| [21] |
AGUSTI A, HEDNER J, MARIN JM, et al. Night-time symptoms: a forgotten dimension of COPD[J]. Eur Respir Rev, 2011, 20(121): 183-194.
[DOI]
|
| [22] |
ADETILOYE AO, ERHABOR GE, OBASEKI DO, et al. Impact of sleep quality on the health-related quality of life of patients with chronic obstructive pulmonary disease[J]. West Afr J Med, 2018, 35(3): 173-179.
|
| [23] |
DIGNANI L, TOCCACELI A, LUCERTINI C, et al. Sleep and quality of life in people with COPD: a descriptive-correlational study[J]. Clin Nurs Res, 2016, 25(4): 432-447.
[DOI]
|
| [24] |
张如意, 游秋云, 张舜波, 等. 睡眠及睡眠剥夺与人体免疫系统的相关性探讨[J]. 中华中医药杂志, 2016, 31(10): 4169-4171. [CNKI]
|
| [25] |
BANKS S, DINGES DF. Behavioral and physiological consequences of sleep restriction[J]. J Clin Sleep Med, 2007, 3(5): 519-528.
[DOI]
|
| [26] |
SHOROFSKY M, BOURBEAU J, KIMOFF J, et al. Impaired sleep quality in COPD is associated with exacerbations: the CanCOLD cohort study[J]. Chest, 2019, 156(5): 852-863.
[DOI]
|
| [27] |
胡红, 韩国敬. 哮喘-慢阻肺重叠综合征的诊治进展[J]. 武警医学, 2016, 27(9): 865-870. [DOI]
|
| [28] |
FANG L, GAO P, BAO H, et al. Chronic obstructive pulmonary disease in China: a nationwide prevalence study[J]. Lancet Respir Med, 2018, 6(6): 421-430.
[DOI]
|
 2021, Vol. 48
2021, Vol. 48


