2. 上海市心血管病研究所 上海 200032
2. Shanghai Institute of Cardiovascular Disease, Shanghai 200032, China
心脏黏液瘤是最常见的心脏肿瘤,黏液瘤多发于左心房,占70~80%,而右心房占10%~15%,双心房、左右心室或多腔室占5%~10%[1]。右心房肿瘤常因肿瘤梗阻腔静脉或三尖瓣而出现明显的症状[2],但目前国内外关于右心房黏液瘤报道较少,因此对右心房黏液瘤的临床表现及诊疗体会经验有限。胸骨正中切口是心脏肿瘤切除术的标准入路,而近年来,微创技术在心脏外科领域广泛应用,包括胸骨部分切口、右胸前外侧切口、右腋下直小切口等。本文回顾性分析了复旦大学附属中山医院近些年完成的右心房黏液瘤切除手术,总结其临床表现和两种入路的手术经验报道如下。
资料和方法一般资料 本研究为回顾性临床对比研究,收集2005年5月至2019年12月我院心脏外科收治的单发的右心房黏液瘤共计61例,所有患者术后均经病理诊断明确,根据手术入路分为胸骨正中切口组(胸骨组,n=45)和右胸前外侧切口组(微创组,n=16),其中男性25例,女性36例,年龄19~82岁,平均(53.6±13.4)岁。首发的临床症状为:体检发现22例,胸闷气促不适或胸痛、心悸等19例,头晕、晕厥9例,腔静脉梗阻症状10例。所有患者均行经胸超声心动图明确右心房内占位,对黏液瘤诊断不能明确的患者行心脏MRI和PET-CT以明确肿瘤性质。合并有中度或以上三尖瓣反流5例,合并冠状动脉粥样硬化性心脏病2例,合并高血压16例,合并糖尿病10例。术前NYHA心功能Ⅰ~Ⅱ级40例,Ⅲ级18例,Ⅳ级3例(表 1)。
| (x±s or n) | |||||||||||||||||||||||||||||
| Parameter | MS group (n=45) |
RT group (n=16) |
t or χ2 | P | |||||||||||||||||||||||||
| Age (y) | 54.4±14.1 | 52.0±11.5 | 0.610 | 0.544 | |||||||||||||||||||||||||
| Female | 23 | 13 | 4.433 | 0.035 | |||||||||||||||||||||||||
| BMI (kg/m2) | 23.5±2.2 | 23.2±2.4 | 0.324 | 0.747 | |||||||||||||||||||||||||
| LVEF (%) | 63.5±6.7 | 65.5±5.6 | 1.077 | 0.286 | |||||||||||||||||||||||||
| Clinical symptom | 1.572 | 0.298 | |||||||||||||||||||||||||||
| No symptoms by TTE | 14 | 9 | |||||||||||||||||||||||||||
| Chest discomfort | 15 | 4 | |||||||||||||||||||||||||||
| Dizziness or syncope | 7 | 2 | |||||||||||||||||||||||||||
| Symptoms of vena cava obstruction | 9 | 1 | |||||||||||||||||||||||||||
| Comorbidity | |||||||||||||||||||||||||||||
| Diabetes mellitus | 6 | 4 | 1.172 | 0.279 | |||||||||||||||||||||||||
| Hypertension | 11 | 5 | 0.283 | 0.595 | |||||||||||||||||||||||||
| CADa | 2 | 0 | - | 1.000 | |||||||||||||||||||||||||
| Moderate or more TRa | 4 | 1 | - | 1.000 | |||||||||||||||||||||||||
| NYHA class | 1.098 | 0.275 | |||||||||||||||||||||||||||
| Ⅰ or Ⅱ | 27 | 13 | |||||||||||||||||||||||||||
| Ⅲ | 15 | 3 | |||||||||||||||||||||||||||
| Ⅳ | 3 | 0 | |||||||||||||||||||||||||||
| MS:Median sternotomy;RT:Right mini-thoracotomy;BMI:Body mass index;LVEF:Left ventricular ejection fraction;TTE:Transthoracic echocardiography;CAD:Coronary artery disease;NYHA:New York Heart Association; TR:Tricuspid regurgitation. aFisher’s exact test. | |||||||||||||||||||||||||||||
手术方法 所有患者采用全身麻醉、气管插管,取仰卧位,置入食管超声心动图(transthoracic echocardiography, TEE)术中监测。
胸骨组经由胸骨正中切口完成手术,其经由主动脉、上下腔静脉插管建立体外循环后,大部分患者采用主动脉阻断后切开右心房完成黏液瘤切除术(部分患者在体外循环下不阻断升主动脉行不停跳心脏手术),仔细探查肿瘤附着部位,尽可能彻底切除肿瘤及附着蒂部心内膜及心肌组织,术中同时探查三尖瓣反流情况,根据病变情况行三尖瓣瓣环成形术,合并冠心病患者行冠状动脉旁路移植术。微创组经右胸前外侧切口(4~5 cm)第4肋间进胸手术,具体手术方法见我们之前的报道[3]。
术后处理及随访 术后患者被送至心脏外科重症监护室(ICU),待其完全清醒、自主呼吸有力、动脉血气指标正常后拔除气管插管。大多数患者待术后第一天血流动力学稳定且呼吸平稳后返普通病房,一般引流量 < 150 mL/d后拔除引流管,鼓励患者早期下床活动,恢复顺利者术后3~6天可出院,术后12个月复查经胸超声心动图随访。
统计学方法 采用SPSS 22.0统计学软件对数据进行分析。正态分布的计量资料用x±s表示,采用独立样本t检验进行比较;非正态分布计量资料用M(IQR)表示,采用秩和检验进行比较;分类计数资料以频数及百分比表示,采用χ2检验进行比较(不满足χ2检验条件者行Fisher确切概率法计算);双侧检验以P < 0.05为差异有统计学意义。
结果所有患者均经病理切片确诊为黏液瘤,术后无院内死亡,无再次开胸止血、脑血管意外、肾功能衰竭等严重并发症。胸骨组1例合并冠心病同期行冠状动脉旁路移植术后持续低氧血症,经机械通气辅助3天后脱机。胸骨组有2例出现胸骨愈合不良,2例出现新发房颤,经保守治疗后均好转,胸骨组其他患者和微创组所有患者恢复可。两组平均心肺转流时间相似,但微创组平均手术时间、主动脉阻断时间均较胸骨组缩短,术后平均机械通气时间、ICU时间和术后住院时间也均减少,差异有统计学意义。微创组的引流量较胸骨组明显减少,73.8%(45/61)的患者住院期间未接受任何血制品的输注,微创组仅1例住院期间需血制品输注,明显少于胸骨组。
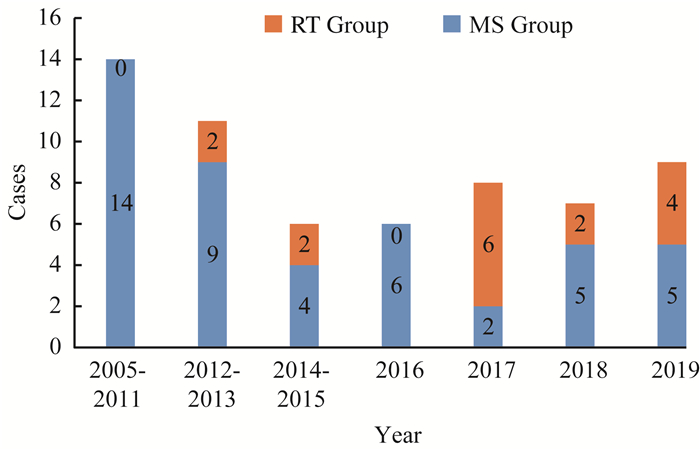
45例患者采用胸骨正中切口完成肿瘤切除手术,而16例患者经由右胸前外侧第4肋间切口完成手术,图 1显示复旦大学附属中山医院2005年至2019年两种入路行右心房黏液瘤手术切除的分布情况,近3年微创入路占50%(10/20)。其中微创组2例中转胸骨正中切口,分别因为肿瘤太大暴露困难和右侧胸腔严重黏连,余患者均按原切口完成手术,13例患者在体外循环辅助心脏不停跳下切除右心房黏液瘤,其中微创组3例。患者肿瘤蒂部附着于右心房游离壁25例,房间隔22例,上、下腔静脉附近9例,三尖瓣瓣环附近5例,肿瘤及蒂部内膜下切除14例(微创组和胸骨组分别为9例和5例),缺损的右心房或房间隔组织以补片修补23例(微创组和胸骨组分别为18例和5例),同期行三尖瓣瓣环成形术5例(微创组和胸骨组分别为4例和1例),胸骨组有2例患者行冠状动脉旁路移植术(表 2)。
|
| 图 1 两种手术入路历年分布情况 Fig 1 Surgical distribution over the years |
| (x±s or n) | |||||||||||||||||||||||||||||
| Parameters | MS group | RT group | t /χ2 | P | |||||||||||||||||||||||||
| Length of incision (mm) | 16.2±1.8 | 4.5±0.5 | 25.640 | < 0.001 | |||||||||||||||||||||||||
| Extend incision or conversion to MS | - | 2 | - | - | |||||||||||||||||||||||||
| CPB time (min) | 48.9±10.2 | 44.3±9.3 | 1.588 | 0.118 | |||||||||||||||||||||||||
| On-pump beating heart techniquea | 10 | 3 | - | 1.000 | |||||||||||||||||||||||||
| Cross-clamp time (min) | 23.0±5.7 | 16.1±5.3 | 3.884 | < 0.001 | |||||||||||||||||||||||||
| Operation time (min) | 165.1±17.8 | 146.3±14.5 | 3.806 | < 0.001 | |||||||||||||||||||||||||
| Location of the myxoma | 1.844 | 0.605 | |||||||||||||||||||||||||||
| Atrial septum | 14 | 8 | |||||||||||||||||||||||||||
| Free wall of atrial | 20 | 5 | |||||||||||||||||||||||||||
| Adjacent vena cava | 7 | 2 | |||||||||||||||||||||||||||
| Adjacent tricuspid annulus | 4 | 1 | |||||||||||||||||||||||||||
| Concomitant surgery | 0.878 | 0.645 | |||||||||||||||||||||||||||
| Tricuspid valve repair | 4 | 1 | |||||||||||||||||||||||||||
| CABG | 2 | 0 | |||||||||||||||||||||||||||
| Submucosal dissection | 9 | 5 | 0.845 | 0.358 | |||||||||||||||||||||||||
| Patch technique | 18 | 5 | 0.385 | 0.535 | |||||||||||||||||||||||||
| Mortalitya | 0 | 0 | - | 1.000 | |||||||||||||||||||||||||
| Ventilation time (h) | 7.8±4.3 | 5.0±3.4 | 2.253 | 0.028 | |||||||||||||||||||||||||
| ICU length of stay (h) | 17.3±7.8 | 14.1±7.0 | 1.435 | 0.156 | |||||||||||||||||||||||||
| Postoperative hospital length of stay (d) | 7.1±2.0 | 5.3±1.7 | 3.196 | 0.002 | |||||||||||||||||||||||||
| Drainage | 520.1±219.3 | 365.0±136.8 | 2.657 | 0.010 | |||||||||||||||||||||||||
| Drainage retention time | 2.9±0.8 | 1.8±0.6 | 4.847 | < 0.001 | |||||||||||||||||||||||||
| Composite adverse outcomesa | 5 | 0 | - | 0.313 | |||||||||||||||||||||||||
| Transfusiona | 15 | 1 | - | 0.350 | |||||||||||||||||||||||||
| MS:Median sternotomy;RT:Right mini-thoracotomy;CPB:Cardiopulmonary bypass;CABG:Coronary artery bypass grafting;ICU:Intensive care unit. aFisher’s exact test. | |||||||||||||||||||||||||||||
术后随访3~153个月,随访率95.6%,1例患者随访期间非心源性死亡,余患者恢复良好,随访超声心动图未见肿瘤复发。
讨论国外文献报道心脏肿瘤尸检发生率为0.001%~0.19%,良性肿瘤占心脏肿瘤的75%,良性肿瘤中黏液瘤占50%,其余有脂肪瘤、弹力纤维瘤或横纹肌瘤[4]。黏液瘤好发于任何年龄,但常见于30~60岁人群,女性多见,人群中黏液瘤散发多见,亦有家族性黏液瘤文献报道[5]。我们统计了复旦大学附属中山医院2005—2019年手术治疗的心脏黏液瘤共845例,其中单纯起源于右心房61例,约占7.2%,与国内外文献报道类似。国内阜外心血管病医院总结近30年494例心脏肿瘤,其中黏液瘤432例(87.4%),男性187例,女性245例,单发于左心房388例(89.8%),右心房21例(4.9%),心室或多发黏液瘤23例(5.3%)[6]。韩劲松等[7]总结中国医科大学1980—2004年收治的232例原发性心脏肿瘤的临床资料,黏液瘤218例(94.0%),其中200例(91.7%)位于左心房,右心房12例(5.5%),其他腔室6例(2.8%),数据与本中心统计结果相似。
左心房黏液瘤蒂部多附着于房间隔,李德强等[8]报道11例右心房黏液瘤,其中9例蒂部附着于房间隔,本组61例右心房黏液瘤中22例患者蒂部附着于房间隔,25例附着于右心房游离壁,与文献报道类似,术中应仔细探查肿瘤蒂部,尽可能彻底切除肿瘤及附着蒂部心内膜及心肌组织,部分肿瘤附着于重要解剖结构不能全部切除,则切除肿瘤蒂部至正常健康组织后低功率电灼蒂部周围正常心肌组织,视缺损心内膜或心肌组织范围予4-0聚丙烯带垫片直接缝合或取心包补片修补;对于蒂部较宽导致切除心房壁或房间隔范围较大,需仔细考量直接缝合产生的张力,必要时取心包重建右心房壁或房间隔。
目前微创手术可应用于多种心脏手术,如二尖瓣手术[9]、三尖瓣手术[10]、先天性心脏病纠治术,并可经多种微创入路,如右胸前外侧切口[9]、右腋下直小切口[11]、胸骨上段或下段切口[12]等。右胸前外侧切口保留了胸骨完整性,可充分暴露主动脉瓣根部、上下腔静脉、左右心房等,且切口隐蔽、美容效果好,因此应用最为广泛,结合我们微创二尖瓣手术的经验,我们逐步尝试经右胸前外侧切口第4肋间入胸行心脏肿瘤切除术,目前已完成近170例,其中黏液瘤位于右心房16例,参考我院2005—2019年的单纯右心房黏液瘤手术径路的演变趋势(图 1),采用微创入路手术的比例逐步升高。本研究对比了两种手术入路的临床资料,发现两组患者术前资料无明显差异,但微创组手术时间、术后机械通气时间和ICU时间等均较胸骨组缩短,且减少术后引流量、缩短引流管留置时间与术后住院时间和降低输血率,手术安全有效。本组另有13例患者手术在体外循环辅助下心脏不停跳完成,特别对于肿瘤蒂部附着于右心房游离壁,预计术中不需要切开左心房的患者特别适合微创心脏不停跳右心房黏液瘤切除术,可明显缩短手术时间,减小手术创伤,加快术后恢复。
右心房黏液瘤症状和体征特异性差,患者往往未有任何不适症状,待瘤体增大至出现腔静脉或三尖瓣阻塞症状就诊,本组有10例合并腔静脉梗阻症状,因此在建立体外循环时术者必须通过术前心超或术中TEE明确肿瘤部位,避免腔静脉插管时损伤肿瘤,导致瘤体破裂脱落甚至种植。可根据瘤体部位确定插管方式:若瘤体靠近下腔静脉,可采用股静脉插管并在TEE引导下使头端位于下腔静脉右心房结合部以下、肝静脉以上水平;若瘤体靠近上腔静脉,可由麻醉科采用Selding方法穿刺后插管,既能方便腔静脉阻断后引流,又能避免损伤瘤体,颈内静脉穿刺后插管可以减少术后血肿发生率[13]。
黏液瘤多为良性,但有临床复发的可能,目前一般认为肿瘤切除不全、肿瘤种植、脱落栓塞和黏液瘤恶性化有关[14],多发生于术后4年内。本组61例患者随访3~153个月,无1例复发,可能与本组患者尽可能全层完整切除有关,且右心房血液流速慢,肿瘤不易脱落种植或栓塞,术后病理亦未见黏液瘤恶性化,且与本组随访时间较短有关。右心房肿瘤术前需与原发性心脏恶性肿瘤或转移性恶性肿瘤鉴别诊断,两者均多发于右心房。原发性心脏恶性肿瘤往往瘤体活动度差,蒂部相对宽泛且固定,常累及心肌组织,经体表超声心动图多可鉴别,转移性恶性肿瘤多有原发恶性肿瘤病史,特别是肾癌、肝癌等,常易沿下腔静脉瘤栓转移至右心房,若患者有肾癌、肝癌等恶性肿瘤病史,必须高度怀疑为转移性恶性肿瘤,必要时可行心脏MRI或PET-CT明确肿瘤性质[15],但最终诊断仍需术后病理分析。另外,黏液瘤需与血管内平滑肌瘤病鉴别,该肿瘤多原发于盆腔,经下腔静脉侵袭性生长至右心房[16],本中心有1例拟诊右心房黏液瘤术中反复探查未见右心房内肿瘤附着部,只见肿瘤自下腔静脉长入右心房,术后病理确诊为血管内平滑肌瘤病,术后盆腔MRI发现原发病灶。
本文总结分析比较我院在过去15年间以两种手术入路行右心房黏液瘤切除术的手术效果,不足之处在于:第一,本研究属于单中心回顾性病例对照研究,样本量较小,可能对结果产生偏倚;第二, 两组患者手术时间段差异明显,微创手术入路集中在2012年以后,两组直接对比可能会有诸多因素导致结果的偏倚;第三, 本文比较分析两种术式近期手术效果,远期效果仍待进一步随访。
综上,右心房黏液瘤手术治疗效果好,术后中远期复发率低。采用右胸前外侧微创切口进行手术,可缩短手术时间,减少手术创伤。
| [1] |
REYNEN K. Cardiac myxomas[J]. N Engl J Med, 1995, 333: 1610-1617.
[DOI]
|
| [2] |
SHAPIRO LM. Cardiac tumours:diagnosis and management[J]. Heart, 2001, 85(2): 218-22.
[DOI]
|
| [3] |
宋凯, 沈金强, 魏来, 等. 微创技术在心脏肿瘤外科治疗中的临床应用[J]. 中国胸心血管外科临床杂志, 2017, 24(8): 626-629. [URI]
|
| [4] |
BUTANY J, NAIR V, NASEEMUDDIN A, et al. Cardiac tumors:diagnosis and management[J]. Lancet Oncol, 2005, 6(4): 219-228.
[DOI]
|
| [5] |
BRUCE CJ. Cardiac tumours:diagnosis and management[J]. Heart, 2011, 97(2): 151-160.
[DOI]
|
| [6] |
胡盛寿, 王小啟, 许建屏, 等. 心脏肿瘤外科治疗经验总结[J]. 中华医学杂志, 2006, 86(11): 766-770. [DOI]
|
| [7] |
韩劲松, 安君, 阎德民. 原发性心脏肿瘤232例临床分析[J]. 中华外科杂志, 2006, 44(2): 87-89. [DOI]
|
| [8] |
李德强, 阎德民, 萧德绵. 右心房黏液瘤外科治疗体会[J]. 中华胸心血管外科杂志, 2002, 18(1): 41. [DOI]
|
| [9] |
魏来, 沈金强, 王春生, 等. 三种入路行二尖瓣后叶成形手术近中期疗效比较[J]. 中华外科杂志, 2012, 50(7): 637-641. [DOI]
|
| [10] |
MAIMAITI A, WEI L, YANG Y, et al. Benefits of a right anterolateral minithoracotomy rather than a median sternotomy in isolated tricuspid redo procedures[J]. J Thorac Dis, 2017, 9(5): 1281-1288.
[DOI]
|
| [11] |
王东进, 吴清玉, 杨秀滨, 等. 微创心脏瓣膜替换术73例报告[J]. 中华外科杂志, 1999, 37(4): 243-244. [DOI]
|
| [12] |
沈金强, 魏来, 夏利民, 等. 右胸骨旁横切口和胸骨上段切口行微创主动脉瓣置换术的临床对比研究[J]. 中华外科杂志, 2016, 54(8): 601-604. [DOI]
|
| [13] |
周荻, 罗红. 微创心脏手术建立体外循环时经皮上腔静脉插管技术[J]. 中华麻醉学杂志, 2011, 31(6): 1500. [URI]
|
| [14] |
NAVID S, SARMAD S, ABBASALI K. Mitral valve recurrence of a left atrial myxoma[J]. Eur J Cardiothorac Surg, 2002, 21(3): 568-573.
[DOI]
|
| [15] |
MOTWANI M, KIDAMBI A, HERZOG BA, et al. MR imaging of cardiac tumors and masses:a review of methods and clinical applications[J]. Radiology, 2013, 268(1): 26-43.
[DOI]
|
| [16] |
HUA L, DEMIN X, WEIQI L, et al. Complete resection of intracardiac leiomyomatosis through an abdominal approach under peripheral cardiopulmonary bypass[J]. J Thorac Cardiovasc Surg, 2016, 152(4): 91-93.
[DOI]
|
 2020, Vol. 47
2020, Vol. 47


