2. 复旦大学附属妇产科医院护理部 上海 200011
2. Department of Nursing, Obstetrics and Gynecology Hospital, Fudan University, Shanghai 200011, China
妊娠期糖尿病(gestational diabetes mellitus, GDM)是指妊娠期间首次发生或发现的不同程度的葡萄糖耐受不良[1],是常见的妊娠期合并症,全球发病率高达14%[2],而中国发病率更居全球前列[3]。GDM给孕妇及胎儿带来诸多不良影响[4],并增加了个人及社会的医疗负担[5]。目前,GDM常用的治疗策略包括饮食干预、运动干预及胰岛素治疗,其中,胰岛素治疗由于其胰岛素大分子不能透过胎盘组织影响胎儿,一直被视为GDM孕妇经饮食和运动干预效果不理想后的标准用药[1]。然而,胰岛素治疗存在给药方式复杂繁琐、易引起妊娠期低血糖、增加孕期体重、患者依从性差等缺点[6]。而口服降糖药由于服药方便,无需注射而逐渐受到关注,目前国际上主要使用的口服降糖药包括二甲双胍和格列苯脲[7]。随着GDM口服药物临床试验不断完善,相关系统评价得以迅速发展,其治疗的安全性及有效性方面的证据也逐渐增多,但不同的系统评价在结局指标、文献质量、分析方法、证据等级等方面有所差异,缺乏全面、系统的汇总评估。系统评价再评价是全面收集同一疾病或同一健康问题的治疗或病因、诊断、预后等方面的相关系统评价,并对其进行综合研究的一种方法[8]。本研究旨在通过系统评价再评价,评估口服降糖药治疗GDM的安全性及有效性,为临床医务人员提供决策依据。
资料和方法纳入标准 (1)研究类型:包括随机对照试验(RCT)的系统评价或meta分析;(2)研究对象:经75 g口服葡萄糖耐量试验诊断为GDM且经非药物治疗后效果不佳需药物治疗控制血糖的孕妇,国家、种族和年龄不限;(3)干预措施:试验组采用格列苯脲/二甲双胍(单独用药或结合胰岛素用药),对照组采用胰岛素治疗/安慰剂;(4)结局指标:有效性评估指标包括空腹血糖、餐后血糖、孕晚期HbA1c等血糖控制结果;安全性评估指标包括孕期及分娩后GDM妇女及胎儿不良结局及并发症发生率;(5)语种为中、英文。
排除标准 (1)重复发表的文献;(2)与GDM孕妇口服降糖药格列苯脲或二甲双胍治疗无关的其他文献;(3)会议摘要或无法获取全文的文献。
文献检索策略 计算机检索The Cochrane Library、The Joanna Briggs Institute Library、EMBASE、PubMed、中国生物医学数据库(CBM)、中国知网(CNKI)、万方数据库(WANFANG)、维普数据库(VIP)。检索采用主题词和自由词结合的方式,英文关键词包括“gestational diabetes, diabetes in pregnancy, hyperglycemia, insulin resistance, glucose intolerance, oral antidiabetic agents,oral hypoglycemic agents, OAD, OHA, metformin, glibenclamide, glyburide,systematic review, meta-analysis”;中文关键词包括“妊娠,孕期,糖尿病,高血糖,胰岛素抵抗,葡萄糖耐受不良,口服降糖药,二甲双胍,格列苯脲,系统评价,meta分析,荟萃分析”。检索时间限定为从建库至2018年11月。
文献筛选与资料提取 由2名研究者分别阅读文题、摘要,对可能符合纳入标准的文献进一步阅读全文进行筛选,如遇分歧,讨论或咨询具备更高循证资质的第三方决定。采用Excel表格对最终纳入的文献进行资料提取,提取内容包括作者、发表年份、纳入研究类型、纳入研究数量及研究对象数量、干预和对照措施、纳入研究质量评价方法、结局指标、主要结论等。对于不同系统评价中重复纳入的相同原始研究,均以先发表文献中的数据为主,从而避免同一组数据反复计算,如有必要确认或补充数据,则参考原始文献。
文献质量评价和证据分级 由2名研究者分别采用系统评价的评价工具AMSTAR(A Measurement Tool to Assess Systematic Reviews)对纳入系统评价的方法学质量进行评价。采用推荐分级的评价、制定与评估工具GRADE(Grades of Recommendations Assessment,Development and Evaluation)对结局指标进行证据质量评价。如遇分歧,讨论或咨询第三方。
资料分析方法 考虑到本次研究纳入的系统评价/meta分析临床一致性较好,研究结果数据采用RevMan5软件进行定量分析。二分类变量效应量采用相对危险度(RR)及95%CI;连续性变量采用均数差(mean difference, MD)及95%CI。通过χ2检验判断是否存在异质性,P>0.1、I2<50%则选择固定效应模型分析;P≤0.1、I2 ≥50%,则选择随机效应模型。效应量概率值P≤0.05表示合并的效应量有统计学意义,P>0.05则合并的效应量无统计学意义。单项系统评价的结果或部分无法提取进行合并的数据则采用描述性分析。
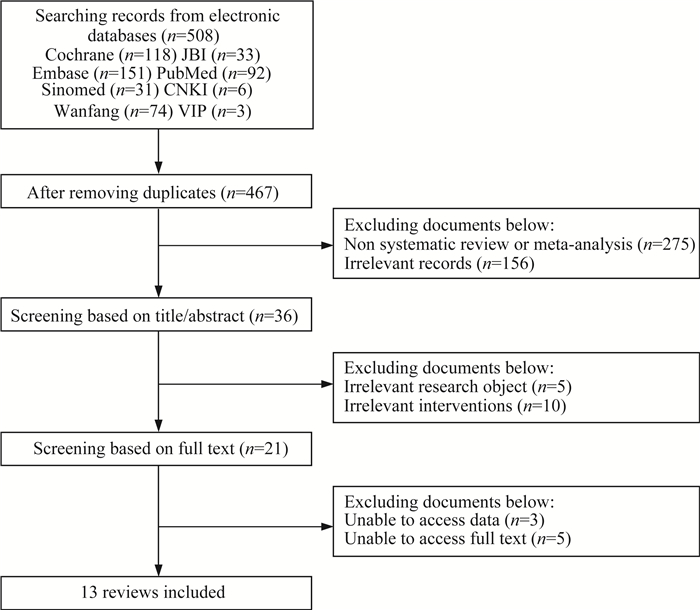
结果文献筛选流程及结果 共检索到文献508篇,去除重复后获得467篇,阅读文题和摘要筛选,并阅读全文,排除研究类型、研究对象不符以及结果无法提取、无法获得全文等文献,最终纳入13篇。文献筛选流程见图 1。
|
| 图 1 文献检索和筛选流程 Fig 1 Flow chart of the systematic literature search and selection |
纳入研究的基本特征 纳入研究均为公开发表的文献,其中学位论文1篇,中文期刊文献3篇,英文期刊文献9篇,发表时间为2010~2017年。纳入的系统评价中,9篇比较了二甲双胍与胰岛素治疗GDM的效果,3篇比较了二甲双胍/格列苯脲与胰岛素的效果,1篇比较了二甲双胍/格列苯脲与胰岛素/安慰剂的效果。各系统评价中纳入的原始研究重复率较高,13篇系统评价共包含120项研究,可纳入的研究为109项,去除重复后纳入31项RCT研究。在对纳入RCT偏倚风险评价中,有9篇采用Cochrane系统推荐的偏倚风险评估工具,1篇采用Jadad量表,1篇采用QUADAS量表,2篇采用的偏移风险评估工具不详。纳入研究的基本特征见表 1。
| Reviews | RCT included | Sample size | Treatment | Quality assessment | Main Conclusion | |
| Intervention | Control | |||||
| Dhulkotia[9] 2010 | 6 | 1 388 | metformin/glyburide | Insulin | Unclear | There are no differences in glycemic control or pregnancy outcomes when OHAs were compared with insulin |
| Zhang[10] 2011 | 4 | 872 | metformin (alone or complemented with insulin) | Insulin analogues, insulin monotherapies, sulfonylureas, a-glycosidase inhibitors, or other oral hypoglycemic agents | Cochrane Risk of Bias Tool | Metformin will not increase the incidence of adverse perinatal outcomes and will not have adverse effect on the growth and development of the fetus, but it can cause adverse reaction in alimentary tract |
| Gui[11] 2013 | 5 | 1 270 | metformin | Insulin | Unclear | Metformin is comparable with insulin in glycemic control and neonatal outcomes. It might be more suitable for women with mild GDM. |
| Poolsup[12] 2014 | 13 | 2 151 | metformin/glyburide | Insulin | Cochrane Risk of Bias Tool | The available evidence suggests favorable effects of metformin in treating GDM patients. Metformin seems to be an efficacious alternative to insulin and a better choice than glyburide especially those with mild form of disease |
| Ruan[13] 2014 | 7 | 1 564 | metformin | Insulin | Cochrane Risk of Bias Tool | Metformin can reduce the risk of hypoglycemia in newborns, and metformin is safe for newborns |
| Zhao[14] 2015 | 8 | 1 592 | metformin | Insulin | Cochrane Risk of Bias Tool | There is no clinically relevant difference in efficacy or safety between metformin and insulin; however, metformin may be a good choice for GDM because of the lower risk of PIH. |
| Kitwitee[15] 2015 | 8 | 1 712 | metformin | Insulin | Cochrane Risk of Bias Tool | In women with gestational diabetes, metformin use and insulin therapy have comparable glycemic control profile, but metformin use was associated with lower risk of neonatal hypoglycemia |
| Li[16] 2015 | 11 | 2 712 | Metformin | Insulin | QUADAS | Metformin can significantly reduce several adverse maternal and neonatal outcomes including PIH rate, incidence of hypoglycemia and NICU, thus it may be an effective and safe alternative or additional treatment to insulin for GDM women |
| Zhang[17] 2015 | 16 | 2 665 | Metformin/Glyburide | Insulin | Cochrane Risk of Bias Tool | Metformin can control blood glucose and maternal weight gain better and lower glycosylated hemoglobin level without increasing maternal hypoglycaemia,but it may significantly shorten gestational age. |
| Zhu[18] 2016 | 8 | 1 712 | Metformin | Insulin | Jadad scale | Metformin may be beneficial in treating gestational diabetes. |
| Feng[19] 2017 | 12 | 3 046 | Metformin | Insulin | Cochrane Risk of Bias Tool | According to most maternal and neonatal outcomes, metformin is an effective and safe alternative to insulin for GDM patients |
| Brown[20] 2017 | 13 | 1 487 | 1)Oral anti-diabetic pharmacological therapies vs.placebo/standard care; 2)Metformin vs.glibenclamide; 3)Glibenclamide vs.acarbose; 4)Glibenclamide with or without metformin vs.metformin with or without glibenclamide |
Cochrane Risk of Bias Tool | Short- and long-term clinical outcomes for this review were inadequately reported or not reported. Current choice of oral anti-diabetic pharmacological therapy appears to be based on clinical preference, availability and national clinical practice guidelines | |
| Geng[21] 2015 | 7 | 1 562 | Metformin | Insulin | Cochrane Risk of Bias Tool | In maternal and neonatal outcomes, metformin is comparable with insulin, even has advantages on some aspects. Furthermore, it possesses high security, and imposes no adverse effects on pregnant women and newborns |
方法学质量评价结果 AMSTAR评价结果显示,纳入的系统评价总体方法学质量仍有待提高。所有条目中,有4个条目被评定为报告完整(100%),分别为条目2(纳入研究的选择和数据提取可重复性)、条目3(实施广泛全面的文献检索)、条目7(评价和报道纳入研究的科学性)、条目9(合成纳入研究结果的方法恰当)。而纳入的系统评价最大的方法学质量缺陷主要为缺乏前期设计方案、未考虑纳入文献的发表情况、未列出排除文献清单以及未说明相关利益冲突。具体评价结果见表 2。
| Systematic review | Ⅰ1 | Ⅰ2 | Ⅰ3 | Ⅰ4 | Ⅰ5 | Ⅰ6 | Ⅰ7 | Ⅰ8 | Ⅰ9 | Ⅰ10 | Ⅰ11 |
| Ruan[13], 2014 | N | Y | Y | N | N | Y | Y | Y | Y | Y | N |
| Li[16], 2015 | N | Y | Y | N | N | Y | Y | Y | Y | Y | Y |
| Poolsup[12], 2014 | N | Y | Y | N | N | Y | Y | Y | Y | Y | N |
| Feng[19], 2017 | N | Y | Y | N | N | Y | Y | Y | Y | Y | Y |
| Kitwitee[15], 2015 | Y | Y | Y | N | N | Y | Y | Y | Y | Y | Y |
| Zhao[14], 2015 | N | Y | Y | N | N | Y | Y | Y | Y | Y | Y |
| Zhu[18], 2016 | N | Y | Y | N | N | Y | Y | Y | Y | N | Y |
| Gui[11], 2013 | N | Y | Y | N | N | Y | Y | Y | Y | N | Y |
| Dhulkotia[9], 2010 | Y | Y | Y | Y | N | Y | Y | Y | Y | Y | N |
| Zhang[10], 2011 | N | Y | Y | Y | N | N | Y | N | Y | N | N |
| Zhang[17], 2015 | N | Y | Y | N | N | Y | Y | Y | Y | Y | N |
| Brown[20], 2017 | Y | Y | Y | Y | Y | Y | Y | Y | Y | Y | Y |
| Geng[21], 2015 | N | Y | Y | N | N | Y | Y | Y | Y | Y | N |
| Y:Yes; N:No; Ⅰ1:Was an ‘a priori’ design provided?Ⅰ2:Was there duplicate study selection and data extraction?Ⅰ3:Was a comprehensive literature search performed?Ⅰ4:Was the status of publication (i.e.grey literature) used as an inclusion criterion?Ⅰ5:Was a list of studies (included and excluded) provided?Ⅰ6:Were the characteristics of the included studies provided?Ⅰ7:Was the scientific quality of the included studies assessed and documented?Ⅰ8:Was the scientific quality of the included studies used appropriately in formulating conclusions?Ⅰ9:Were the methods used to combine the findings of studies appropriate?Ⅰ10:Was the likelihood of publication bias assessed?Ⅰ11:Was the conflict of interest stated? | |||||||||||
主要结局指标及证据质量分级 本研究纳入的系统评价包括二甲双胍与胰岛素比较,格列苯脲与胰岛素比较,以及口服降糖药(格列苯脲)与安慰剂比较(尚无二甲双胍与安慰剂比较的系统评价),主要结局指标共38项,其中2个结局指标为高质量,13个为中等质量,14个为低质量,9个为极低质量。重要结局指标分析如下。
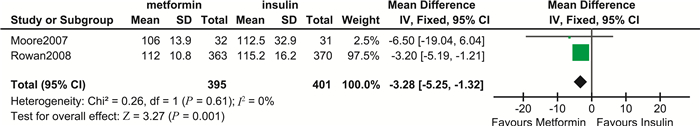
二甲双胍vs.胰岛素 4项研究报告了二甲双胍与胰岛素比较的空腹血糖水平,2项研究报告了餐后血糖水平,5项研究报告了孕晚期HbA1c水平。结果显示,与胰岛素治疗相比,使用二甲双胍的孕妇空腹血糖水平(MD=-0.33,95%CI:-1.77~1.11,P=0.65)及孕晚期HbA1c水平(MD=0.03,95%CI:-0.09~0.15,P=0.65)均无显著差异,但实验组孕妇餐后血糖水平明显低于对照组,且合并效应量差异具有统计学意义(MD=-3.28,95%CI:-5.25~-1.32,P=0.001),证据质量低,见图 2。敏感性分析结果显示森林图结构未发生改变,但合并效应无统计学意义(MD=-6.50,95%CI:-19.04~6.04,P=0.31)。
|
| 图 2 二甲双胍与胰岛素治疗GDM餐后血糖水平比较森林图 Fig 2 Forest plot of postprandial blood glucose comparing metformin with insulin in treating GDM |
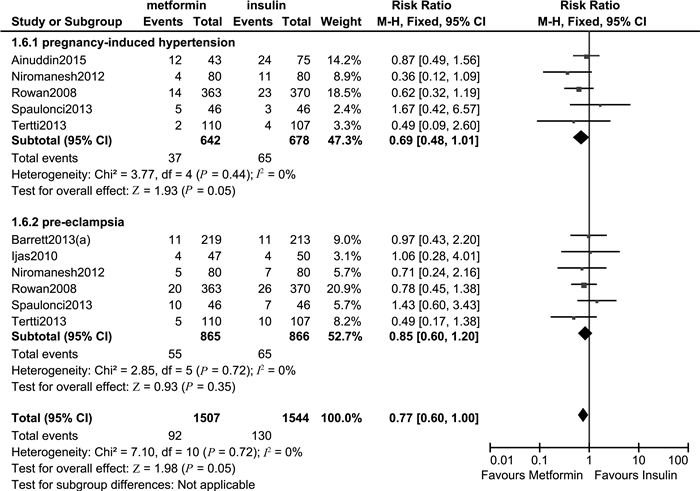
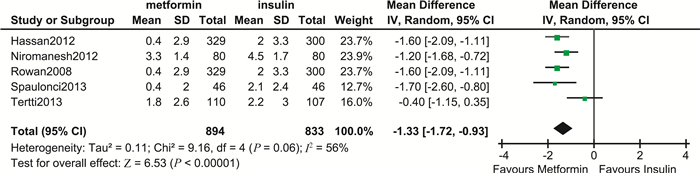
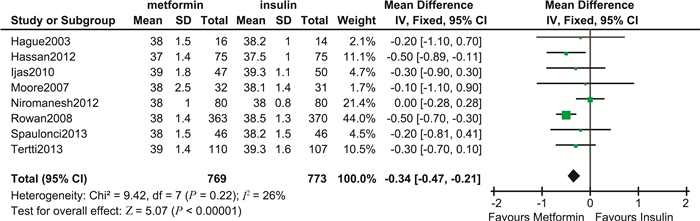
孕产妇结局 研究报告的孕产妇主要结局指标包括入组后体重增加、剖宫产、妊娠高血压、子痫前期、妊娠时限及早产。结果显示,二甲双胍组剖宫产发生率(RR=0.93, 95%CI:0.83~1.04,P=0.20)、子痫前期发生率(RR=0.85,95%CI:060~1.20,P=0.35)、早产发生率(RR=1.26,95%CI:0.89~1.79,P=0.19)与胰岛素组差异均无统计学意义。然而,二甲双胍组妊娠高血压发生倾向更低(RR=0.69,95%CI:0.48~1.01,P=0.05),差异具有统计学意义,证据质量高,见图 3。孕妇入组后体重增加(MD=-1.33,95%CI:-1.72~-0.93,P<0.000 01)及妊娠时限(MD=-0.34,95%CI:-0.47~-0.21,P<0.000 01)均低于胰岛素组,差异具有统计学意义,证据质量分别为低质量和中等质量(图 4~5)。其中,妊娠时限的敏感性分析结果显示森林图结构未发生改变,且合并效应仍具有统计学意义(MD=-0.21,95%CI:-0.38~-0.03,P<0.02)。
|
| 图 3 二甲双胍与胰岛素治疗GDM妊娠期高血压综合征发生率比较森林图 Fig 3 Forest plot of hypertensive disorder comparing metformin with insulin in treating GDM |
|
| 图 4 二甲双胍与胰岛素治疗GDM孕妇入组后体重增加比较森林图 Fig 4 Forest plot of weight gain after randomization comparing metformin with insulin in treating GDM |
|
| 图 5 二甲双胍与胰岛素治疗GDM孕妇妊娠时限比较森林图 Fig 5 Forest plot of gestational age comparing metformin with insulin in treating GDM |
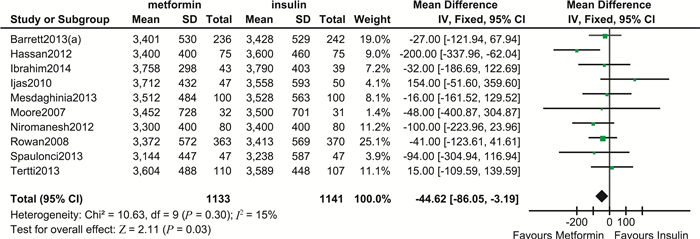
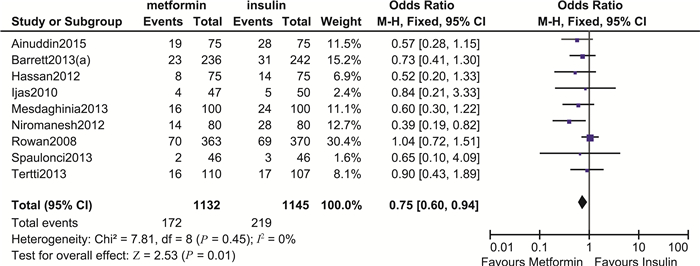
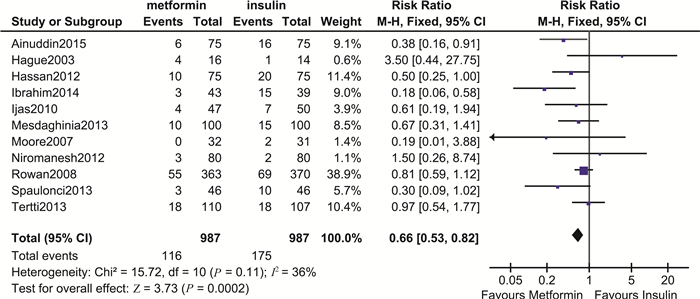
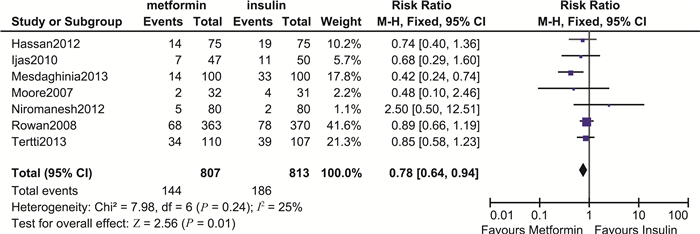
围生儿结局 围生儿主要结局指标包括出生体重、巨大儿、大于胎龄儿(large for gestational age, LGA)、小于胎龄儿(small for gestational age, SGA)、新生儿低血糖、高胆红素血症、新生儿入住ICU、呼吸窘迫综合征和围生儿死亡率等。meta分析结果显示,二甲双胍组与胰岛素组相比其巨大儿发生率(RR=0.92,95%CI:0.73~1.16,P=0.48)、SGA发生率(RR=1.08,95%CI:0.81~1.43,P=0.60),高胆红素血症发生率(RR=0.83,95%CI:0.64~1.08,P=0.16)、RDS发生率(RR=0.80,95%CI:0.53~1.19,P=0.27)及围生儿死亡率(RR=0.99,95%CI:0.14~7.06,P=1.00)差异均无统计学意义。但二甲双胍组新生儿出生体重更低(MD=-44.62,95%CI:-86.05~-3.19,P=0.03),差异具有统计学意义,证据质量为中等。同时,二甲双胍组LGA的发生率也更低(RR=0.75,95%CI:0.60~0.94,P=0.01),差异具有统计学意义,证据质量为中等。此外二甲双胍组新生儿低血糖(RR=0.66,95%CI:0.53~0.82,P=0.000 2)以及新生儿入住ICU率(RR=0.78,95%CI:0.64~0.94,P=0.01)均显著低于胰岛素组,差异均具有统计学意义,证据质量分别为中等质量和低质量(图 6~9)。新生儿低血糖的敏感性分析结果显示森林图结构未发生改变,且合并效应仍具有统计学意义(RR=0.57,95%CI:0.42~0.76,P=0.000 1)。新生儿入住ICU率的敏感性分析结果显示森林图结构未发生改变,且合并效应仍具有统计学意义(RR=0.70,95%CI:0.54~0.90,P=0.006)。
|
| 图 6 二甲双胍与胰岛素治疗GDM新生儿出生体重比较森林图 Fig 6 Forest plot of birth weight comparing metformin with insulin in treating GDM |
|
| 图 7 二甲双胍与胰岛素治疗GDM大于胎龄儿发生率比较森林图 Fig 7 Forest plot of large for gestational age comparing metformin with insulin in treating GDM |
|
| 图 8 二甲双胍与胰岛素治疗GDM新生儿低血糖发生率比较森林图 Fig 8 Forest plot of neonatal hypoglycemia comparing metformin with insulin in treating GDM |
|
| 图 9 二甲双胍与胰岛素治疗GDM新生儿入ICU率比较森林图 Fig 9 Forest plot of neonatal intensive care admission comparing metformin with insulin in treating GDM |
格列苯脲vs.胰岛素 与胰岛素组相比,格列苯脲组治疗后孕妇空腹血糖(MD=2.15,95%CI: -0.08~4.37,P=0.06)、餐后血糖(MD=-3.53,95%CI:-2.44~9.50,P=0.25)及孕晚期HbA1c水平(MD=0.10,95%CI:-0.03~0.23,P=0.12)差异均无统计学意义。
孕产妇结局 格列苯脲组孕妇入组后体重增加(MD=-0.67,95%CI:-1.69~0.36,P=0.2)、剖宫产发生率(RR=0.88,95%CI:0.71~1.11,P=0.28)、子痫前期发生率(RR=1.13,95%CI:0.60~2.16,P=0.70)及早产发生率(RR=1.04,95%CI:0.50~2.16,P=0.92)均与胰岛素组相当。格列苯脲组孕妇低血糖发生率更低(RR=0.36, 95%CI:0.02~5.64,P=0.46),差异无统计学意义。
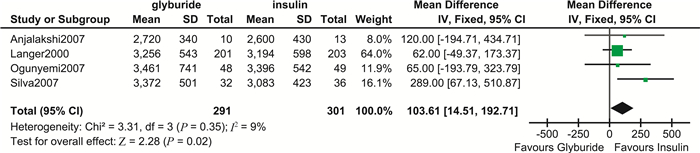
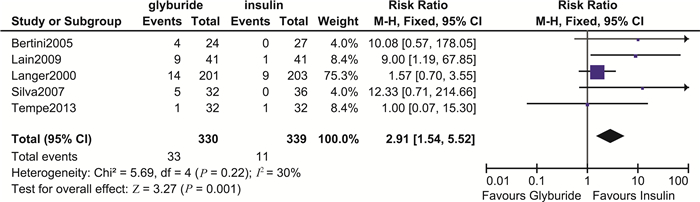
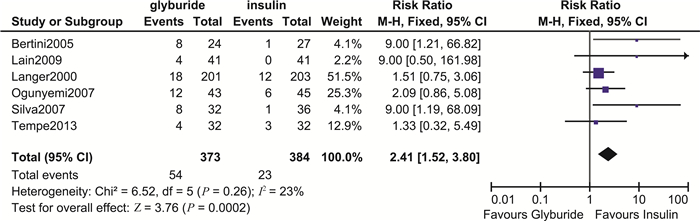
围生儿结局 格列苯脲组小于胎龄儿发生率(RR=1.06,95%CI:0.21~5.30,P=0.94)及围生儿死亡率(RR=1.68,95%CI:0.40~6.94,P=0.45)与胰岛素组差异均无统计学意义。但值得注意的是,格列苯脲组LGA(RR=2.86,95%CI:0.87~9.41,P=0.08)发生倾向更高,但差异无统计学意义。此外,格列苯脲组新生儿出生体重(MD=103.61,95%CI:14.51~192.71,P=0.02)高于胰岛素组,且差异具有统计学意义,证据质量中等(图 10);同时,其敏感性分析结果显示森林图结构未发生改变,且合并效应仍具有统计学意义(MD=177.61,95%CI:29.10~326.11,P=0.02)。此外,格列苯脲组发生巨大儿(RR=2.91,95%CI:1.54~5.52,P=0.001)及新生儿低血糖(RR=2.41,95%CI:1.52~3.80,P=0.000 2)的风险更高,差异均具有统计学意义,证据质量分别为中等质量和极低质量(图 11、12)。巨大儿发生率的敏感性分析结果显示森林图结构未发生改变,且合并效应仍具有统计学意义(RR=6.99,95%CI:2.14~22.86,P=0.001)。新生儿低血糖发生率的敏感性分析也结果显示森林图结构未发生改变,且合并效应仍具有统计学意义(RR=3.35,95%CI:1.80~6.25,P=0.000 1)。
|
| 图 10 格列苯脲与胰岛素治疗GDM新生儿出生体重比较森林图 Fig 10 Forest plot of birth weight comparing glyburide with insulin in treating GDM |
|
| 图 11 格列苯脲与胰岛素治疗GDM巨大儿发生率比较森林图 Fig 11 Forest plot of macrosomia comparing glyburide with insulin in treating GDM |
|
| 图 12 格列苯脲与胰岛素治疗GDM新生儿低血糖发生率比较森林图 Fig 12 Forest plot of neonatal hypoglycemia comparing glyburide with insulin in treating GDM |
格列本脲vs.安慰剂 纳入的系统评价中,仅1篇比较了口服降糖药与安慰剂的效果,该系统评价纳入了1篇研究,共375例研究对象,比较了格列苯脲与安慰剂的作用。系统评价结果显示,格列苯脲降低孕期血糖水平(RR=-3.00, 95%CI:-5.13~-0.87, P=0.005 7),差异具有统计学意义但证据质量低。目前尚无证据表明格列本脲和安慰剂组在妊娠高血压疾病(RR=1.24, 95%CI:0.81~1.90, P=0.33)(极低质量)、剖宫产(RR=1.03, 95%CI:0.79~1.34,P=0.84)(极低质量)、会阴损伤(RR=0.98, 95%CI:0.06~15.62,P=0.99)(极低质量)、引产(RR=1.18, 95%CI:0.79~1.76,P=0.42)(极低质量)等方面存在差异,也尚无数据显示口服降糖药组与安慰剂组比较其LGA的发生率(RR=0.89, 95%CI:0.51~1.58,P=0.71)存在差异,证据质量低。其他孕产妇及围生儿结局指标也均未报道存在显著差异。
讨论口服降糖药治疗妊娠期糖尿病有效性评估 传统的GDM药物治疗是指皮下注射胰岛素,为弥补其给药方式复杂繁琐、易引起妊娠期低血糖、增加孕期体重、患者依从性差等缺点[6],越来越多的权威机构将口服降糖药纳入孕期降糖药物的考虑之列。苏格兰校际指南网络(Scottish Intercollegiate Guidelines Network, SIGN)2013年指南[22]、新西兰临床实践指南研究组(New Zealand Guideline Group, NZGG) 2014年指南[23]等已将口服降糖药(格列苯脲/二甲双胍)与胰岛素同列为孕期用药选择。2015年,英国国家健康与临床优选研究所(National Institute for Health and Care Excellence, NICE)发布的指南中,更推荐口服降糖药二甲双胍作为优于胰岛素的首选药物[7]。尽管如此,我国临床上对GDM孕妇使用口服降糖药仍存在诸多争议。因此,为便于临床工作人员作出最优决策,有必要对现有的口服降糖药物治疗效果研究进行梳理和归纳。纳入的系统评价中,9篇比较了二甲双胍与胰岛素治疗GDM的效果,3篇比较了二甲双胍/格列苯脲与胰岛素的效果,1篇比较了二甲双胍/格列苯脲与胰岛素/安慰剂的效果。结果显示,与胰岛素相比,二甲双胍在空腹血糖、孕晚期HbA1c水平方面与胰岛素组并无显著差异,在餐后血糖控制方面优于胰岛素,格列苯脲组与安慰剂组比较其血糖水平显著降低,与胰岛素组比较血糖控制水平则无显著差异。尽管现有证据已证实了二甲双胍或格列苯脲对GDM血糖控制的有效性,但口服降糖药是否可作为替代药物及选择何种口服降糖药仍需考虑药物对孕妇及胎儿的短期及长期影响。
口服降糖药治疗妊娠期糖尿病的安全性评估 安全性是孕期药物选择的关键性因素,按化学结构,二甲双胍属于双胍类药物,通过抑制肝糖原异生和肠壁细胞摄取葡萄糖,同时促进周围组织细胞对葡萄糖的吸收和利用而发挥作用[24],而格列苯脲属第二代磺酰脲类药物,主要通过增强胰岛素分泌来发挥作用[25]。两者分子量均小于胰岛素大分子,需重点考量其胎盘透过性。已有研究显示,格列苯脲具有较低的胎盘透过率[26],而二甲双胍则可自由通过胎盘[27],可能会对胎儿造成一定的影响。本研究分析了口服降糖药对孕期及分娩后GDM妇女及胎儿并发症发生率的影响。结果显示,与胰岛素治疗相比,二甲双胍治疗组能降低孕妇入组后体重增加,缩短妊娠时限,妊娠期高血压的发病率也更低。同时,二甲双胍组新生儿出生体重更低,且LGA、新生儿低血糖、入住ICU率等结局也显著改善。尽管一篇系统评价提示二甲双胍可能增加早产风险,但本文经过系统的数据整合后显示,二甲双胍治疗组与胰岛素治疗组早产发生风险并无统计学差异(P=0.19)。因此,现有研究表明,对于孕妇及胎儿而言,二甲双胍不会增加短期不良妊娠结局的发生,且对孕妇及胎儿可能存在潜在的益处,提示其是适合GDM孕妇的合理选择[14]。但值得注意的是,格列苯脲治疗组新生儿出生体重更高,且其巨大儿及新生儿低血糖的发生率也显著增加,提示格列苯脲可能给新生儿造成短期的不良影响,使用时应考虑到可能发生的不良反应。此外,纳入研究中尚无口服降糖药对孕妇及胎儿远期影响的研究,仍需通过大量的临床研究及更长时间的随访来观察药物对胎儿生长发育以及未来长远的影响。
口服降糖药系统评价的方法学质量 系统评价是循证医学重要的研究方法和最佳证据的重要来源,被视为评价临床疗效、制订临床指南和规范的基石[28]。然而,只有经过严格质量控制的系统评价,才能为临床实践和卫生决策提供尽可能减少偏倚和接近真实的科学证据[29]。本研究采用AMSTAR工具对纳入的13篇系统评价进行方法学质量评价,结果显示,纳入系统评价总体方法学质量有待提高,这可能与纳入的文章多为个人发表,缺乏如Cochrane严格完善的系统评价质量保证系统有关。纳入的系统评价中,有77%的系统评价没有提供前期设计方案,可能影响系统评价构建过程的严谨性;77%的系统评价未说明发表情况是否已考虑在纳入标准中,可能缺失对未发表的阴性研究报告、会议论文摘要、各种简报、学位论文等的检索,存在发表偏倚的风险[30];91.7%的系统评价未说明是否提供排除研究的文献清单,这可能与一般学术刊物上存在版面限制,编辑不大可能把较为冗长的排除文献列于论文后相关[28]。此外,41.7%的系统评价在利益关系和冲突的报告中存在缺陷,可能潜在影响结果的客观性。
口服降糖药证据强度 系统评价方法学质量并不代表证据质量,为帮助系统评价的使用者准确理解和正确应用该系统评价提供的证据,本研究采用GRADE系统对结局指标进行证据质量分级,以评估我们对效应估计值正确的把握程度[31-32]。按照GRADE系统降级依据,本研究对纳入的13项系统评价(其中1项系统评价原文中已采用GRADE系统分级)共38个结局指标进行了证据质量评价。结果显示,2个结局指标为高质量,13个为中等质量,14个为低质量,9个为极低质量,提示口服降糖药的有效性和安全性仍需开展大样本高质量研究。5个降级因素中,主要降级因素是研究的局限性和不精确性,研究的局限性降级提示系统评价纳入的RCT在研究设计方面仍存在一定缺陷[33],如随机化过程的缺失;而研究的不精确性降级则体现在效应量估计值的可信区间过宽,未达到最优信息样本量[34]。这些缺陷在很大程度上降低了系统评价结论的可信度,特别是对于一些关键性结局指标,如餐后血糖水平为低质量,说明二甲双胍控制餐后血糖水平优于胰岛素的这一结果有待更大样本量证据的检验。
结语 现有临床研究证据表明,口服降糖药二甲双胍和格列苯脲在控制血糖效果上和胰岛素无明显差异,二甲双胍餐后血糖控制效果甚至优于胰岛素治疗效果。在药物安全性方面,二甲双胍并不增加围生期不良妊娠结局的风险,且对孕妇及胎儿可能存在潜在的益处,而格列苯脲则可能增加新生儿不良结局的风险。目前,尚无数据说明口服降糖药格列苯脲或二甲双胍对孕妇及胎儿的远期影响。本研究认为针对口服降糖药有效性和安全性的系统评价其方法学质量总体不高,结论的证据水平普遍为低或中等,尽管这对结论会造成一定影响,但考虑到本次研究重新将纳入的系统评价/meta分析中的研究结果数据采用RevMan5软件进行定量分析,极大程度降低了这一风险,也保证了本研究结论的可信度。
此外,纳入文献中均未提及不同严重程度的GDM是否需要采用不同的治疗策略,以及服药剂量与服药时间对结局的影响,这也为以后的研究提供了更加详细的方向。对于不同的结局指标,其临床意义差异较大,如婴儿的体重、剖宫产率也可能与人种、文化差异相关,且由于语种限制,可能尚有非中、英文的研究呈现不同的结果。因此,临床工作人员在使用证据时需综合考虑患者情况,基于自身临床情景,充分考量可能出现的不良影响,综合作出决策。同时,通过本文的讨论,也期待有更多高质量的随机对照试验提供更加可靠的证据。
| [1] |
中华医学会妇产科学分会产科学组中华医学会围产医学分会妊娠合并糖尿病协作组. 妊娠合并糖尿病诊治指南(2014)[J]. 中华妇产科杂志, 2014, 49(8): 561-569. [DOI]
|
| [2] |
THE INTERNATIONAL DIABETES FEDERATION.International Diabetes Federation.IDF Diabetes Atlas 8th Edition[EB/OL].(2017-12-14) [2019-02-20].https://www.idf.org/e-library/welcome.html.
|
| [3] |
关怀, 尚丽新. 妊娠期糖尿病流行现状[J]. 中国实用妇科与产科杂志, 2015, 31(1): 91-94. [URI]
|
| [4] |
CATALANO PM, MCINTYRE HD, CRUICKSHANK JK, et al. The hyperglycemia and adverse pregnancy outcome study:associations of GDM and obesity with pregnancy outcomes[J]. Diabetes Care, 2012, 35(4): 780-786.
[DOI]
|
| [5] |
LENOIR-WIJNKOOP I, BEEK EMVAN DER, GARSSEN J, et al. Health economic modeling to assess short-term costs of maternal overweight, gestational diabetes, and related macrosomia-a pilot evaluation[J]. Front Pharmacol, 2015, 6: 103.
[URI]
|
| [6] |
曾雅畅, 李慕军, 陈悦. 二甲双胍对妊娠期糖尿病治疗效果的系统评价[J]. 中国妇幼保健, 2013, 28(35): 5906-5909. [URI]
|
| [7] |
NATIONAL COLLABORATING CENTRE FOR WOMEN'S AND CHILDREN'S HEALTH.Diabetes in pregnancy: Management of diabetes and its complications from preconception to the postnatal period[EB/OL].(2015-02-16)[2019-02-20].https://www.nice.org.uk/guidance/ng3.
|
| [8] |
刘雅莉, 袁金秋, 杨克虎, 等. 系统评价再评价的制作方法简介及相关资料分析[J]. 中国循证儿科杂志, 2011, 6(1): 58-64. [DOI]
|
| [9] |
DHULKOTIA JS, OLA B, FRASER R, et al. Oral hypoglycemic agents vs. insulin in management of gestational diabetes:a systematic review and meta-analysis[J]. Am J Obstet Gynecol, 2010, 203(5): 451-457.
|
| [10] |
张文慧, 米娜瓦尔·霍加, 董旭南. 二甲双胍治疗妊娠糖尿病的系统评价[J]. 中国全科医学, 2011(6): 592-595. [DOI]
|
| [11] |
GUI J, LIU Q, FENG L. Metformin vs. insulin in the management of gestational diabetes:a meta-analysis[J]. PLoS One, 2013, 8(5): e64585.
[DOI]
|
| [12] |
POOLSUP N, SUKSOMBOON N, AMIN M. Efficacy and safety of oral antidiabetic drugs in comparison to insulin in treating gestational diabetes mellitus:a meta-analysis[J]. PLoS One, 2014, 9(10): e109985.
[DOI]
|
| [13] |
阮冠宇, 许秋星, 蔡慧雅, 等. 二甲双胍与胰岛素对母亲妊娠期糖尿病新生儿安全性的系统评价[J]. 中国临床药理学与治疗学, 2014(10): 1139-1143. [URI]
|
| [14] |
ZHAO LP, SHENG XY, ZHOU S, et al. Metformin versus insulin for gestational diabetes mellitus:a meta-analysis[J]. Br J Clin Pharmacol, 2015, 80(5): 1224-1234.
[DOI]
|
| [15] |
KITWITEE P, LIMWATTANANON S, LIMWATTAN-ANON C, et al. Metformin for the treatment of gestational diabetes:An updated meta-analysis[J]. Diabetes Res Clin Pract, 2015, 109(3): 521-532.
[DOI]
|
| [16] |
LI G, ZHAO S, CUI S, et al. Effect comparison of metformin with insulin treatment for gestational diabetes:a meta-analysis based on RCTs[J]. Arch Gynecol Obstet, 2015, 292(1): 111-120.
[DOI]
|
| [17] |
张杰, 张华, KAMANAKC, 等. 二甲双胍和格列苯脲在妊娠期糖尿病中的安全性和有效性评价:网络Meta分析[J]. 重庆医科大学学报, 2015, 40(2): 289-295. [URI]
|
| [18] |
ZHU B, ZHANG L, FAN YY, et al. Metformin versus insulin in gestational diabetes mellitus:a meta-analysis of randomized clinical trials[J]. Ir J Med Sci, 2016, 185(2): 371-381.
[DOI]
|
| [19] |
FENG Y, YANG H. Metformin——a potentially effective drug for gestational diabetes mellitus:a systematic review and meta-analysis[J]. J Matern Fetal Neonatal Med, 2017, 30(15): 1874-1881.
[DOI]
|
| [20] |
BROWN J, MARTIS R, HUGHES B, et al. Oral anti-diabetic pharmacological therapies for the treatment of women with gestational diabetes[J]. Cochrane Database Syst Rev, 2017(1): No.:CD011967.
|
| [21] |
耿飞飞.二甲双胍与胰岛素治疗妊娠期糖尿病的疗效及安全性系统评价[D].新疆医科大学内科学(内分泌与代谢病学), 2015.
|
| [22] |
SCOTTISH INTERCOLLEGIATE GUIDELINES NETWORK.Management of diabetes: A national clinical guideline[EB/OL].(2013-11-10)[2019-02-20].http://www.sign.ac.uk/assets/sign116.pdf.
|
| [23] |
Ministry Of Health. Screening, Diagnosis and Management of Gestational Diabetes in New Zealand:A clinical practice guideline[M]. Wellington: Ministry of Health, 2014.
|
| [24] |
VIOLLET B, GUIGAS B, SANZ GN, et al. Cellular and molecular mechanisms of metformin:an overview[J]. Clin Sci (Lond), 2012, 122(6): 253-270.
[DOI]
|
| [25] |
COUSTAN DR, BARBOUR L. Insulin vs.Glyburide for gestational diabetes[J]. JAMA, 2018, 319(17): 1769-1770.
[DOI]
|
| [26] |
端木雯婧, 黄桦, 姚勤, 等. 格列苯脲在人胎盘中转运机制的研究状况[J]. 中国临床药理学杂志, 2016, 32(3): 283-285. [URI]
|
| [27] |
NGUYEN L, CHAN SY, TEO AKK. Metformin from mother to unborn child- are there unwarranted effects?[J]. EBio Medicine, 2018, 35: 394-404.
[URI]
|
| [28] |
熊俊, 陈日新. 系统评价/Meta分析方法学质量的评价工具AMSTAR[J]. 中国循证医学杂志, 2011, 11(9): 1084-1089. [DOI]
|
| [29] |
PUSSEGODA K, TURNER L, GARRITTY C, et al. Systematic review adherence to methodological or reporting quality[J]. Syst Rev, 2017, 6(1): 131.
[URI]
|
| [30] |
AERT RCMVAN, WICHERTS JM, ASSEN MALMVAN. Publication bias examined in meta-analyses from psychology and medicine:A meta-meta-analysis[J]. PLoS One, 2019, 14(4): e0215052.
[DOI]
|
| [31] |
BALSHEMH, HELFANDAM, SCHUNEMANNHJ, 等. GRADE指南:Ⅲ.证据质量分级[J]. 中国循证医学杂志, 2011, 11(4): 451-455. [DOI]
|
| [32] |
陈耀龙, 姚亮, SUSANNORRIS, 等. GRADE在系统评价中应用的必要性及注意事项[J]. 中国循证医学杂志, 2013, 13(12): 1401-1404. [DOI]
|
| [33] |
GUYATTGH, OXMANAD, VISTG, 等. GRADE指南:Ⅳ.证据质量分级——研究的局限性(偏倚风险)[J]. 中国循证医学杂志, 2011, 11(4): 456-463. [DOI]
|
| [34] |
GUYATTGH, AD.OXMAN, KUNZR, 等. GRADE指南:Ⅵ.证据质量评价——不精确性(随机误差)[J]. 中国循证医学杂志, 2011, 11(12): 1435-1443. [DOI]
|
 2020, Vol. 47
2020, Vol. 47


