作为一种无创、检测方便的生物标志物呼出气一氧化氮(fractional exhaled nitric oxide,FeNO)是气道T2型炎症生物标志物和气道高反应性的替代指标,不仅对哮喘的诊断、治疗评估及预后判断具有重要的意义,还对咳嗽变异性哮喘、嗜酸粒细胞(eosinophil,EOS)性支气管炎和急性EOS性肺炎以及变态反应性肺部疾病的病因辅助诊断和治疗指导具有参考意义[1-3]。
FeNO分析仪的测量方法主要包括化学发光法和电化学法。化学发光法灵敏度高、响应快、重复性好,被认为是FeNO检测的标准方法[3-5],但仪器体积较大、价格贵且需频繁校准,限制了其临床应用。电化学法基于电化学传感器原理,检测快、体积小、便于携带且操作简便。随着检测技术的发展,越来越多类型的FeNO分析仪被应用于临床,其中NIOX VERO(美国Circassia公司)电化学检分析仪逐渐成为行业的金标准;另一方面,不同电化学分析仪器的测量结果可在一定范围内或经过转换后在临床交叉使用,有助于慢性气道疾病治疗、随访、干预和管理[6-12]。
BA200(浙江亿联康医疗科技有限公司)是一种检测FeNO的新型电化学分析仪,尚未与其他类型FeNO分析仪进行比对。本研究选用了目前国内广泛应用的电化学分析仪NIOX VERO为参照,通过比较两者测量NO标准气和FeNO数值的差异,评价两种分析仪的性能异同和测定一致性,探讨BA200的创新性及其在临床的应用价值。
资料和方法研究对象和分组 收集2021年10月至11月间在复旦大学附属中山医院呼吸科门诊就诊并开具FeNO检查的患者预约名单,按照每日预约时间编号,由软件进行随机选择,共选择210例受试者。其中23例受试者由于配合不佳或其他问题拒绝进行对照试验测定,最终187例受试者入组,分别用FeNO分析仪BA200和NIOX VERO进行测定。同样由软件随机选择其中50例受试者进行重复性分析试验,其余137例受试者进行一致性分析试验。所用患者均知情同意,该研究经中山医院伦理委员会审查通过,批件号为B2019-248(3)。
FeNO测定 两种电化学分析仪BA200与NIOX VERO的技术参数如表 1所示。所有的FeNO测量过程都严格遵照指南[7-9]的质控要求进行,呼出气流速控制在(50±5)mL/s。根据BA200本身的测量要求,每日检测前、环境变化或操作者认为需要时进行仪器校准,测量过程中操作者根据测量曲线复核呼气流速剔除不符合标准的曲线。
| Parameter | BA200 | NIOX VERO |
| Accuracy(×10-9) | < 50×10-9:±2.5×10-9 ≥50×10-9:±5.0% |
< 50 ×10-9:±5×10-9 ≥50 ×10-9:±10% |
| Repeatibility | < 50×10-9:SD < 1.5×10-9 ≥50×10-9:RSD < 3.0% |
< 30×10-9:SD < 3×10-9 ≥30×10-9:RSD < 10% |
| Testing time | 35 s | 70 s |
| Detection limit | 1×10-9 | 5×10-9 |
| Measuring range | (0-4 000)×10-9 | (5-300)×10-9 |
| Filter tip | Mask-type filter | Mouth-type filter |
试验方法
标准气测定 先用42i型化学发光法氮氧化物分析仪(美国ThermoFisher Scientific公司)对NO标准气(法国Air Liquide公司)进行标定1次,再使用BA200与NIOX VERO两种型号的电化学分析仪对低、中、高3个浓度(20×10-9、70×10-9、200×10-9)的NO标准气测量3次。根据FeNO临床检测的分布选择的低、中、高3个浓度的标准气,尽可能地涵盖临床检测的FeNO范围。
一致性研究 随机、先后使用BA200与NIOX VERO对137例患者进行FeNO测量,试验过程中,同一患者连续测量至少间隔30 min[4]。
重复性研究 随机先后使用BA200与NIOX VERO对50例患者进行3次FeNO重复测量。试验过程中,同一患者连续测量至少间隔30 min。
统计学分析 本研究使用SPSS 22.0软件进行统计分析,Matlab软件进行作图。标准气测量的准确度用相对误差描述,精密度用标准偏差(SD)或相对标准偏差(RSD)描述。测量数值的重复性和一致性分别采用组内相关系数(intraclass correlation coefficient,ICC)和Bland-Altman方法进行分析。使用ROC曲线比较两种分析仪在不同临界值的灵敏度和特异度。
结果标准气测量 分选用了低、中、高3个浓度(20×10-9、70×10-9、200×10-9)的NO标准气体,经标定后浓度分别为19.5×10-9、70.5×10-9和208.0×10-9。根据BA200与NIOX VERO对这3个浓度标准气测量数据计算得到相对误差、SD或RSD(表 2)。测量低浓度NO标准气时,与NIOX VERO相比,BA200的准确度略低,而精密度略高。测量中、高浓度NO标准气时,BA200的准确度和精密度更高。
| (x±s) | |||||||||||||||||||||||||||||
| Index | Strandard gas concentration | ||||||||||||||||||||||||||||
| 20(19.5)×10-9 | 70(70.5)×10-9 | 200(208.0)×10-9 | |||||||||||||||||||||||||||
| NIOX VERO | BA200 | NIOX VERO | BA200 | NIOX VERO | BA200 | ||||||||||||||||||||||||
| FeNO(×10-9) | 18.7±0.58 | 18.6±0.49 | 64.7±2.52 | 69.4±0.10 | 197.3±2.31 | 205.0±0.15 | |||||||||||||||||||||||
| Relative error | -4.3% | -4.8% | -8.3% | -1.6% | -5.1% | -1.5% | |||||||||||||||||||||||
| RSD | 3.1% | 2.7% | 3.9 | 0.1% | 1.2% | 0.1% | |||||||||||||||||||||||
| 19.5×10-9,70.5 ×10-9 and 208.0×10-9 were the actual detected gas concentrations. | |||||||||||||||||||||||||||||
一致性研究 137例受试者中包括正常4人、过敏性鼻炎4人、咳嗽24人、慢性阻塞性肺病3人、哮喘80人、哮喘合并鼻炎2人、支气管炎12人、胸闷8人。由于各组人数差异较大,且FeNO作为T2型气道炎症生物标志物和气道高反应性的替代指标,测定值主要与气道炎症的严重程度相关。最终按照NIOX VERO的测量结果将137例患者分为3组进行FeNO分析(< 25×10-9组,(25~50)×10-9组,> 50×10-9组)[7, 9]。FeNO < 25×10-9组有68人,NIOX VERO测试值为(15.54±5.32)×10-9,BA200测试值为(17.28±5.41)×10-9。FeNO在(25~50)×10-9组有36人,NIOX VERO测试值为(36.97±6.83)×10-9,BA200测试值为(37.80±7.58)×10-9。FeNO > 50×10-9组有33人,NIOX VERO测试值为(105.73±53.68)×10-9,BA200测试值为(107.32±51.95)×10-9。
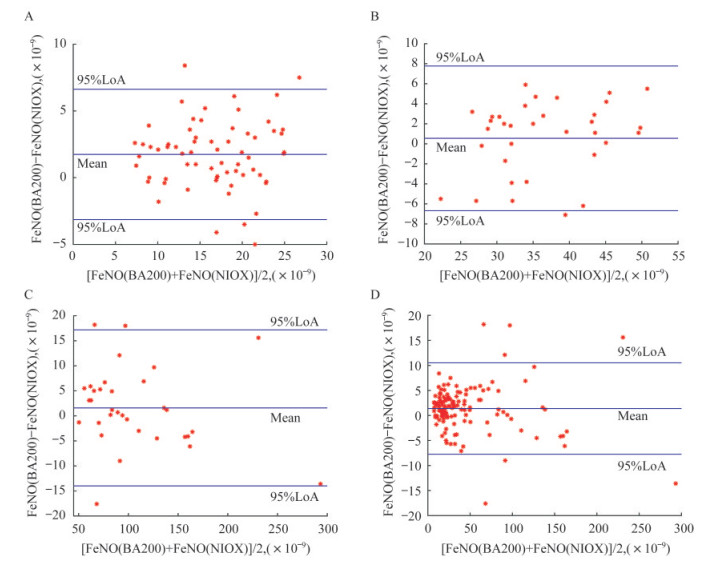
比较NIOX VERO和BA200的测量值,低、中、高浓度组和总体的Bland-Altman分析显示:两者差值的95%一致性界限(limit of agreement,LoA)分别为(-3.239 2~6.724 4)×10-9、(-6.829 0~7.923 4)×10-9、(-14.310 1~17.485 9)×10-9和(-7.922 0~10.704 4)×10-9。绝大部分差值在两者差值均值的95%LoA内(图 1):< 25×10-9组有7.35%(5/68)的点在最大误差范围以外(图 1A);(25~50)×10-9组有2.78%(1/36)的点在最大误差范围以外(图 1B);> 50×10-9组有9.09%(3/33)的点在最大误差范围以外(图 1C);总样本组中有5.11%(7/137)的点在最大误差范围以外(图 1D)。BA200和NIOX VERO测定FeNO均有较好的一致性。
|
| A: FeNO < 25×10-9; B: 25×10-9 < FeNO < 50×10-9; C: FeNO > 50×10-9; D: Total sample. 图 1 BA200和NIOX VERO两种仪器在不同程度FeNO浓度组别的Bland-Altman图 Fig 1 Bland-Altman plots of FeNO by BA200 and NIOX VERO |
重复性研究 入组50例患者,BA200和NIOX的ICC值分别为0.995 3和0.996 8,BA200的ICC值略低于NIOX VERO。二者均大于0.75(P < 0.001),说明BA200和NIOX VERO测量FeNO时的重复性都非常好。
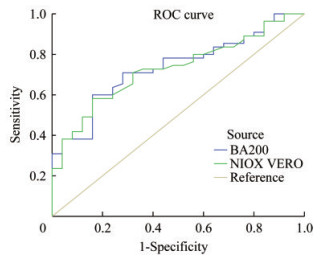
哮喘患者FeNO的ROC曲线分析 本试验中有80例哮喘患者,其中有症状55例,无症状25例,根据有无症状进行ROC曲线分析,图 2显示对BA200和NIOX VERO两种分析仪测量的哮喘患者FeNO数值进行ROC曲线分析,曲线下面积(AUC)分别为0.736(95%CI:0.625~0.846,P=0.001)和0.728(95%CI:0.617~0.839,P=0.001),BA200和NIOX VERO的cut-off值分别为47.65和46.50,当选用49.9作为cut-off值时,BA200和NIOX VERO的灵敏度分别为0.564和0.527,特异度分别为0.840和0.840。根据不同FeNO值得到相应的灵敏度和特异度绘制ROC曲线。
|
| 图 2 哮喘患者有症状ROC曲线分析 Fig 2 Analysis of symptomatic ROC in patients with asthma |
FeNO是无创评估气道炎症的可靠因子,对部分气道反应性炎症疾病尤其是哮喘的诊断和评估有重要参考意义[3-4]。本研究是关于国产电化学分析仪BA200测量FeNO的首次研究,研究中分别对不同浓度NO标准气和呼吸科门诊患者的FeNO进行测量。结果显示,相比于NIOX VERO,BA200具有更高的准确度和精密度,在高、中、低浓度区间均具有较好的一致性,并且BA200的检测速度更快,在临床指导气道过敏性EOS炎症的随访中可以更加方便快捷地得到患者FeNO值。
以往研究中,尚无关于使用NO标准气验证电化学分析仪技术参数的报道。根据指南中FeNO技术标准,仪器的准确度和精密度是测量相关的重要质控因素之一[4-5]。本研究中,在测量低浓度NO标准气时,BA200的精密度略高于NIOX VERO,且二者的精密度和准确度都远远超过指南技术标准[5],甚至符合化学发光法分析仪测量FeNO的技术要求[4]。测量中、高浓度NO标准气时,BA200的相对误差范围缩小到±2%,RSD缩小到±0.1%,其准确度和精密度都达到更高水平。根据研究结果可以认为:BA200仪器具有更优良的准确度和精密度,这是其广泛应用于临床工作的重要前提。
本研究首次用BA200和国内常用的电化学分析仪NIOX VERO进行比较,两者测定FeNO的结果均具有很好的重复性,对50例患者进行重复性试验,经ICC检验分析FeNO值,得到结果为0.995 3和0.996 8,均远大于0.7,统计学上具有显著相关性,两者一致性良好,差异无统计学意义。同时在低、中、高3个测量区间测定的差异性都非常小,测量差值的均值都在2×10-9以内,低于电化学分析器准确度最小范围2.5×10-9。在中等浓度区间里这个差值的均值更小,与指南[8]对化学发光感受器1×10-9的技术要求相当。
将BA200的测量值与NIOX VERO相比,对低、中、高浓度组和总体的Bland-Altman分析显示,两者差值的95%LoA分别为(-3.239 2~6.724 4)×10-9、(-6.829 0~7.923 4)×10-9、(-14.310 1~17.485 9)×10-9和(-7.922 0~10.704 4)×10-9。绝大部分差值在两者差值均值的95%LoA内,说明BA200和NIOX VERO测定同一患者FeNO值时,具有较好的一致性。
根据ROC曲线分析,BA200和NIOX VERO的AUC分别为0.736和0.728,二者的AUC都大于0.700,且BA200的AUC稍大于NIOX VERO,提示在区别哮喘有无症状方面具有相似的鉴别能力。本研究中,ROC曲线分析得到的cut-off值非常接近,BA200和NIOX VERO的cut-off值分别为47.65和46.50,指南和共识都认为成人FeNO > 50×10-9,提示气道EOS性炎症可能性大[2, 13],临床对于哮喘患者2型炎症推荐使用吸入糖皮质激素会更有效控制症状[14]。本研究中选用49.9作为cut-off值时,BA200和NIOX VERO的灵敏度分别为0.564和0.527,特异度分别为0.840和0.840。两者特异度相等,BA200的敏感度高于NIOX VERO,这与BA200仪器本身准确度好、精密度高及其从方法学上对FeNO测量严格质控等因素密切相关。也可以说明两台分析仪对于有症状的哮喘诊断、治疗评估及预后判断有重要意义。
上述两种电化学分析仪测量能保持高度一致性的原因有几方面。第一,测量FeNO前,保证测试环境的稳定,并去除受试者本身因素(如运动和饮食等)的影响[4-5]。第二,避免呼气时漏气是采样过程质控的核心。本研究中BA200分析仪采用的是口罩式滤嘴,减少漏气可能,保证采样过程中呼气流速、时间和呼气压力的真实和稳定[3]。第三,和分析过程质控相关因素相关:(1)本研究观察到BA200的准确度和精密度均符合标准[4]。(2)BA200提供了校准模块,供操作者在每日检测前或环境变化大时进行校准。(3)BA200的测量时间缩短到35 s左右,测量数值可以精确到小数点后一位,仪器的灵敏度更高,检测速度也更快。(4)操作者可以根据BA200的测量曲线复核来保证呼气流速在标准范围内。BA200在方法学上的创新点使其在FeNO测量时质控更加严格,这也成为BA200能够在临床应用的决定性因素。
在国内外关于不同FeNO分析仪的对比评价研究[7-12]中,对于不同的测定结果,研究者分析的原因都和FeNO测定的质控相关。例如:当NIOX VERO仪器与NOA280i仪器比较时,有研究显示NIOX VERO的FeNO测量值总体水平高于NOA280i[7],也有研究显示NIOX VERO的FeNO测定值总体水平低于NOA280i[10],这些差异与传感器类型、定标技术、检测次数、检测先后顺序不同、样本量小或与入组患者疾病类型相关。而在NIOX VERO仪器与Nobreath®仪器[11]的比较中,研究者发现在不同FeNO水平的人群中,结果呈现不一致的规律,其原因也与仪器操作质控有关。在(25~100)×10-9区间内,NIOX VERO与RuiBreath的FeNO测量值具有一致性[8]。NIOX VERO与NIOX MINO的比较[12],两台分析仪的FeNO测定值相近,这和两者相同的检测原理学、操作方法和校准质控紧密相关。在这些研究都得到了相似结果:对于FeNO值的测定,严格把握质控可以提高测定结果的准确性。
本研究侧重BA200的仪器性能和检测方法在临床中的实际应用。通过临床试验发现:在测定气道炎症疾病时,BA200与NIOX VERO具有相同的意义。BA200对于T2型气道炎症和气道高反应性疾病的诊断、治疗评估及预后判断都具有重要的意义:(1)BA200仪器本身有更优良的准确度和精密度;(2)BA200采用口罩式滤嘴,测量过程对呼气流量进行监测和反馈,并增加了校准模块,这些方法学上的创新加强了FeNO测量的质控,更好地保证了检测过程的规范化。(3)BA200和NIOX VERO在测量FeNO时的高度一致性、在区分有症状哮喘的相似临界值都证实了二者可以交叉使用。BA200在临床应用时能为诊断、治疗和预后判断T2型气道炎症和气道高反应性疾病提供便利。(4)由于传感器本身的优势性能,BA200的检测范围为(0~4 000)×10-9,与NIOX VERO相比数据的广度变大,对于临床上测量数值偏大、超出常规测量范围的,尤其是一些气道反应性极高的病例,随访观测中NO值变化更加直观。(5)以往临床检测使用的经典仪器NIOX VERO的检测时间需要70 s,而BA200将检测时间缩短至35 s,检测时间缩短为之前的二分之一。对于需要进行FeNO检测的患者,改良的口罩式滤嘴和质控的加强可以帮助患者更加顺利地完成检测,而更快的检测时间则缩短了患者等待结果的时间,便于快速得到准确结果。随着人们对慢性气道疾病的重视以及相关环境的改变,需要进行FeNO检测的患者数量增加,故排队等候时间较长,而BA200仪器对于检测过程的改良和检测时间的缩短在很大程度上提高了检测效率,减少了患者的等候时间。
本研究仍存在局限性和不足:缺乏对BA200仪器本身稳定性的阶段性观察;缺乏BA200与化学发光分析仪的比较分析;研究样本量不够大;分析时未结合肺功能、血清特异性IgE和血清嗜酸性粒细胞等指标为FeNO测量提供临床参考。
综上所述,BA200电化学分析仪性能良好,方便临床检测,实用性强,可以成为NIOX VERO的临床替代产品,作为国产产品,可以在慢性气道疾病的诊治、随访以及在社区慢性气道疾病管理和防治中发挥更大的作用。
作者贡献声明 薛丽萍,龚颖 试验实施,论文构思、撰写和修改。赵振 试验实施,数据采集,论文修改。胡莉娟,金美龄,宋元林 研究指导,试验实施,论文修订。李丽 研究构思,试验实施和指导,论文修改。
利益冲突声明 所有作者均声明不存在利益冲突。
| [1] |
中华医学会呼吸病学分会哮喘学组. 咳嗽的诊断与治疗指南(2015)[J]. 中华结核和呼吸杂志, 2016, 39(5): 323-354. [DOI]
|
| [2] |
吴克, 王晶, 王培, 等. 呼出气一氧化氮检测在变应性支气管肺曲霉菌病诊疗中的应用[J]. 国际呼吸杂志, 2020, 40(9): 647-650. [DOI]
|
| [3] |
中国医药教育协会慢性气道疾病专业委员会, 中国哮喘联盟. 呼出气一氧化氮检测及其在气道疾病诊治中应用的中国专家共识[J]. 中华医学杂志, 2021, 101(38): 3092-3114. |
| [4] |
AMERICAN THORACIC SOCIETY, EUROPEAN RESPIRATORY SOCIETY. ATS/ERS recommendations for standardized procedures for the online and offline measurement of exhaled lower respiratory nitric oxide and nasal nitric oxide[C]. Am J Respir Crit Care Med, 2005, 171(8): 912-930.
|
| [5] |
HORVÁTH I, BARNES PJ, LOUKIDES S, et al. A European respiratory society technical standard: exhaled biomarkers in lung disease[J]. Eur Respir J, 2017, 49(4): 1600965.
[DOI]
|
| [6] |
KANG SY, LEE SM, LEE SP. Measurement of fractional exhaled nitric oxide in adults: comparison of two different analyzers (NIOX VERO and NO breath)[J]. Tuberc Respir Dis (Seoul), 2021, 84(3): 182-187.
[DOI]
|
| [7] |
ENDO Y, SHIRAI T, AKAMATSU T, et al. Comparison of fractional exhaled nitric oxide levels measured using the NIOX VERO and NOA 280i[J]. Ann Allergy Asthma Immunol, 2017, 119(4): 383-385.
[DOI]
|
| [8] |
LIU Y, CHANG X, LIANG L, et al. A comparative study of the RuiBreath and NIOX VERO analyzers for detecting fractional exhaled nitric oxide[J]. Thorac Dis, 2021, 13(7): 4418-4426.
[DOI]
|
| [9] |
HUANG T, LIU B, YANG D. Fractional exhaled nitric oxide measurement: comparison between the Sunvou-CA2122 analyzer and the NIOX VERO analyzer[J]. Asthma, 2021, 58(1): 52-59.
[DOI]
|
| [10] |
TANABE Y, HARADA N, ITO J, et al. Difference between two exhaled nitric oxide analyzers, NIOX VERO® electrochemical hand-held analyzer and NOA280i® chemiluminescence stationary analyzer[J]. J Asthma, 2019, 56(2): 167-172.
[DOI]
|
| [11] |
INOUE Y, SATO S, MANABE T, et al. Measurement of exhaled nitric oxide in children: a comparison between NObreath® and NIOX VERO® analyzers[J]. Allergy Asthma Immunol Res, 2018, 10(5): 478-489.
[DOI]
|
| [12] |
HARNAN SE, TAPPENDEN P, ESSAT M, et al. Measurement of exhaled nitric oxide concentration in asthma: a systematic review and economic evaluation of NIOX MINO, NIOX VERO and NObreath[J]. Health Techno Assess, 2015, 19(82): 1-330.
|
| [13] |
DWEIK RA, BOGGS PB, ERZURUM SC, et al. An official ATS clinical practice guideline: interpretation of exhaled nitric oxide levels (FENO) for clinical applications[J]. Am J Respir Crit Care Med, 2011, 184(5): 602-615.
[DOI]
|
| [14] |
MURARO A, LEMANSKE RF, HELLINGS PW, et al. Precision medicine in patients with allergic diseases: airway diseases and atopic dermatitis‐PRACTALL document of the European Academy of Allergy and Clinical Immunology and the American Academy of Allergy, Asthma & Immunology[J]. Allergy Clin Immunol, 2016, 137(5): 1347‐1358.
|
 2023, Vol. 50
2023, Vol. 50


