2. 上海市血管病变调控与重塑重点实验室 上海 201399
2. Shanghai Key Laboratory of Vascular Lesions Regulation and Remodeling, Shanghai 201399, China
糖尿病是由遗传和环境因素共同引起的一组以糖代谢紊乱为主要表现的临床综合征,伴多种慢性并发症,导致残疾甚至死亡。2型糖尿病(type 2 diabetes,T2D)占全部糖尿病的90%以上。糖尿病性骨质疏松为糖尿病的重要并发症之一,患者常出现骨量减少、骨强度降低、微结构改变及骨脆性增加,骨折的风险明显增高[1]。近些年越来越多的证据表明,骨也可以作为内分泌器官,调节全身的葡萄糖和能量代谢。骨代谢标志物既能够反映骨细胞的活性,又能够调节相关激素,是骨骼内分泌功能的重要媒介。许小娟等[2]探索了绝经后女性T2D患者骨钙素(osteocalcin,OC)与糖化血红蛋白(glycated hemoglobin,HbA1c)水平的相关性,发现绝经后女性T2D患者OC与HbA1c呈负相关。在老年T2D患者中,OC同样对患者的胰岛素敏感性、胰岛素分泌功能具有积极的调控作用[3]。目前关于骨代谢指标与血糖调控的研究较少且尚无明确定论,此次研究中我们初步探索了中老年T2D患者OC及其他骨代谢指标与HbA1c的关系。
资料和方法研究对象 收集2019年5月—2020年7月在复旦大学附属浦东医院内分泌科住院的符合研究标准的T2D患者共372人,其中男性192人,女性180人。纳入标准:(1)女性为绝经后患者,男性≥45岁;(2)病例数据完整,具有骨代谢指标及骨密度检查结果。排除标准:(1)其他类型糖尿病(1型糖尿病、特殊类型糖尿病、妊娠期糖尿病);(2)继发性骨质疏松(甲状腺及甲状旁腺疾病、肿瘤、使用药物等);(3)既往患甲状腺疾病、甲状腺手术者,各种骨代谢性疾病、既往6个月内存在抗骨质疏松治疗、长期卧床者长期服用糖皮质激素,性激素患者;(4)近半年内使用维生素D、钙剂及激素有关的影响维生素D代谢的药物;(5)近1个月有急性代谢紊乱患者;(6)急性的肝、肾、心脑疾病及精神疾病患者;(7)非自然绝经患者。
研究方法 收集患者一般资料如姓名、年龄、性别、身高、体重、T2D病程、女性绝经年龄、既往病史及用药史、是否有吸烟饮酒史等,并计算身体质量指数(body mass index,BMI)。收集空腹血常规、血脂、肝功能、肾功能、HbA1c、骨代谢指标:25-羟基羟维生素D[25 hydroxy vitamin D,25(OH)D]、β胶原降解产物(特殊序列)(β-C-terminal telopeptide of type I collagen,β-CTX)、骨钙素N端中分子片段(N-terminal osteocalcin,N-MID)、钙(calcium,Ca)、磷(phosphorus,P)指标。双能X线骨密度吸收仪测定左侧股骨颈、髋关节、腰椎L1-L4部位的骨密度(bone mineral density,BMD),单位g/cm²。根据我国2017年出版的2型糖尿病防治指南并结合本研究T2D患者HbA1c水平,将患者并根据血糖控制水平分为3组:A组HbA1c < 7.5%,B组HbA1c 7.5%~8.99%,C组HbA1c≥9.0%。
统计学方法 采用SPSS 26.0和GraphPad Prism v.8软件进行统计分析。计量资料正态分布以x±s表示,当不满足正态分布时以M(Q1,Q3)表示,组间比较采用方差分析,使用LSD-t进行事后检验。Pearson相关性分析探索HbA1c与骨代谢指标相关性。多元线性回归分析探索T2D患者HbA1c的影响因素。T2D病程、N-MID、β-CTX为非正态分布,对数转换后进一步分析。P < 0.05为差异有统计学意义,P < 0.01为差异有显著统计学意义。
结果不同HbA1c水平3组间资料的比较 女性患者中(表 1),3组间年龄、BMI、T2D病程、各部位BMD、25(OH)D、β-CTX及Ca、P指标差异均无统计学意义,N-MID差异有显著统计学意义(P < 0.001)。与C组相比,A组(P < 0.001)及B组(P < 0.001)N-MID水平升高。男性患者中(表 2),3组间年龄、BMI、各部位BMD、25(OH)D、β-CTX、Ca、P指标差异均无统计学意义,T2D病程(P=0.019)、N-MID(P=0.048)差异有统计学意义。与C组相比,B组病程较长(P=0.005),A组N-MID水平升高(P=0.016)。
| (x±s) | |||||||||||||||||||||||||||||
| Variables | Group A HbA1c < 7.5% |
Group B HbA1c 7.5%-8.9% |
Group C HbA1C ≥9.0% |
F | P | ||||||||||||||||||||||||
| N | 34 | 50 | 96 | ||||||||||||||||||||||||||
| Age(y) | 66.71±11.54 | 66.82±10.13 | 66.48±9.62 | 0.020 | 0.980 | ||||||||||||||||||||||||
| BMI(kg/m²) | 24.34±3.35 | 25.35±3.68 | 25.79±3.94 | 1.881 | 0.156 | ||||||||||||||||||||||||
| logT2D course(year) | 0.90±0.34 | 0.99±0.36 | 0.82±0.49 | 2.401 | 0.094 | ||||||||||||||||||||||||
| Lumbar spine BMD(g/cm2) | 0.84±0.15 | 0.89±0.19 | 0.87±0.14 | 0.750 | 0.474 | ||||||||||||||||||||||||
| Femur neck BMD(g/cm2) | 0.66±0.11 | 0.67±0.12 | 0.68±0.12 | 0.402 | 0.670 | ||||||||||||||||||||||||
| Hip joint BMD(g/cm2) | 0.80±0.12 | 0.81±0.15 | 0.83±0.20 | 0.701 | 0.498 | ||||||||||||||||||||||||
| 25(OH)D(ng/mL) | 17.64±5.90 | 19.94±7.21 | 17.88±7.42 | 1.626 | 0.200 | ||||||||||||||||||||||||
| logN-MID(ng/mL) | 1.15±0.17 | 1.15±0.18 | 1.02±0.19 | 11.635 | <0.001 | ||||||||||||||||||||||||
| logβ-CTX(ng/mL) | -0.40±0.20 | -0.43±0.25 | -0.49±0.22 | 2.769 | 0.065 | ||||||||||||||||||||||||
| Ca(mmol/L) | 2.19±0.12 | 2.23±0.11 | 2.20±0.09 | 1.934 | 0.148 | ||||||||||||||||||||||||
| P(mmol/L) | 1.17±0.19 | 1.22±0.16 | 1.17±0.19 | 1.002 | 0.369 | ||||||||||||||||||||||||
| logT2D course:log transformation of T2D course;logN-MID:log transformation of N-MID;logβ-CTX:log transformation of β-CTX. | |||||||||||||||||||||||||||||
| (x±s) | |||||||||||||||||||||||||||||
| Variables | Group A HbA1c < 7.5% |
Group B HbA1c 7.5%-8.9% |
Group C HbA1c ≥9.0% |
F | P | ||||||||||||||||||||||||
| Number | 37 | 49 | 106 | ||||||||||||||||||||||||||
| Age(y) | 64.03±9.36 | 66.41±8.09 | 62.62±9.78 | 2.787 | 0.064 | ||||||||||||||||||||||||
| BMI(kg/m2) | 25.44±3.60 | 25.39±3.36 | 25.14±3.21 | 0.159 | 0.853 | ||||||||||||||||||||||||
| logT2D course(year) | 0.77±0.44 | 0.95±0.37 | 0.73±0.48 | 4.021 | 0.019 | ||||||||||||||||||||||||
| Lumbar spine BMD(g/cm2) | 0.99±0.24 | 1.02±0.19 | 1.03±0.16 | 0.441 | 0.644 | ||||||||||||||||||||||||
| Femur neck BMD(g/cm2) | 0.73±0.17 | 0.78±0.13 | 0.79±0.12 | 2.318 | 0.101 | ||||||||||||||||||||||||
| Hip joint BMD(g/cm2) | 0.89±0.18 | 0.93±0.14 | 0.93±0.13 | 1.166 | 0.314 | ||||||||||||||||||||||||
| 25(OH)D(ng/mL) | 22.74±8.90 | 22.99±6.93 | 21.66±9.78 | 0.446 | 0.641 | ||||||||||||||||||||||||
| logN-MID(ng/mL) | 1.04±0.18 | 1.00±0.14 | 0.97±0.16 | 3.078 | 0.048 | ||||||||||||||||||||||||
| logβ-CTX(ng/mL) | -0.52±0.21 | -0.62±0.30 | -0.55±0.23 | 1.999 | 0.138 | ||||||||||||||||||||||||
| Ca(mmol/L) | 2.20±0.12 | 2.19±0.10 | 2.20±0.11 | 0.138 | 0.871 | ||||||||||||||||||||||||
| P(mmol/L) | 1.13±0.15 | 1.12±0.12 | 1.13±0.21 | 0.029 | 0.972 | ||||||||||||||||||||||||
| logT2D course:log transformation of T2D course;logN-MID:log transformation of N-MID;logβ-CTX:log transformation of β-CTX. | |||||||||||||||||||||||||||||
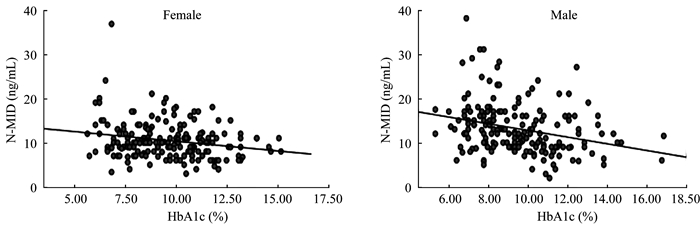
HbA1c与骨代谢指标的相关性分析 Pearson相关性分析结果见表 3和表 4。在女性和男性患者中,HbA1c均与N-MID呈负相关(r=-0.302,P < 0.001;r=-0.207,P=0.004)(图 1),与其他骨代谢指标无相关性。
| Variables | 25(OH)D | logN-MID | logβ-CTX | Ca | P | |||||||||
| r | P | r | P | r | P | r | P | r | P | |||||
| Age | -0.065 | 0.383 | -0.001 | 0.992 | -0.027 | 0.720 | -0.133 | 0.074 | -0.370 | <0.001 | ||||
| BMI | -0.042 | 0.578 | 0.007 | 0.930 | -0.141 | 0.060 | 0.019 | 0.796 | 0.174 | 0.019 | ||||
| logT2D course | 0.021 | 0.777 | -0.062 | 0.411 | -0.188 | 0.011 | -0.049 | 0.512 | -0.153 | 0.040 | ||||
| HbA1c | -0.040 | 0.598 | -0.302 | <0.001 | -0.103 | 0.168 | -0.004 | 0.953 | -0.033 | 0.658 | ||||
| logT2D course:log transformation of T2D course;logN-MID:log transformation of N-MID;logβ-CTX:log transformation of β-CTX. | ||||||||||||||
| Variables | 25(OH)D | logN-MID | logβ-CTX | Ca | P | |||||||||
| r | P | r | P | r | P | r | P | r | P | |||||
| Age | 0.056 | 0.437 | 0.020 | 0.784 | 0.076 | 0.296 | -0.122 | 0.091 | -0.281 | <0.001 | ||||
| BMI | -0.065 | 0.370 | -0.185 | 0.010 | -0.219 | 0.002 | 0.058 | 0.422 | 0.097 | 0.181 | ||||
| logT2D course | -0.020 | 0.785 | -0.107 | 0.141 | -0.245 | 0.001 | -0.018 | 0.806 | -0.101 | 0.163 | ||||
| HbA1c | -0.059 | 0.415 | -0.207 | <0.010 | -0.106 | 0.143 | -0.041 | 0.571 | -0.020 | 0.779 | ||||
| logT2D course:log transformation of T2D course;logN-MID:log transformation of N-MID;logβ-CTX:log transformation of β-CTX. | ||||||||||||||
|
| 图 1 HbA1c与N-MID相关性分析 Fig 1 Correlation analysis between HbA1c and N-MID |
HbA1c影响因素的多元线性回归分析 以HbA1c为因变量,年龄、BMI、T2D病程、25(OH)D、N-MID、β-CTX、Ca、P为自变量行多元线性逐步回归分析。在女性患者中(表 5),T2D病程(β=-0.321,P < 0.001)和N-MID(β=-0.304,P < 0.001)是HbA1c的影响因素。男性患者中(表 6),T2D病程(β=-0.160,P=0.024)、N-MID(β=-0.339,P < 0.001)和β-CTX(β=0.234,P=0.004)是HbA1c的影响因素。
| Variables | HbA1c R2=0.184 P < 0.001 | |||||
| B | SE | β | t | P | 95%CI | |
| logT2D course | -1.559 | 0.348 | -0.304 | -4.474 | <0.001 | -2.246,-0.871 |
| logN-MID | -3.697 | 0.784 | -0.321 | -4.718 | <0.001 | -5.243,-2.151 |
| logT2D course:log transformation of T2D course;logN-MID:log transformation of N-MID. | ||||||
| Variables | HbA1c R2=0.124 P < 0.001 | |||||
| B | SE | β | t | P | 95%CI | |
| logT2D course | -0.738 | 0.325 | -0.160 | -2.273 | 0.024 | -1.378,-0.098 |
| logN-MID | -4.360 | 1.008 | -0.339 | -4.324 | <0.001 | -6.348,-2.371 |
| logβ-CTX | 1.969 | 0.677 | 0.234 | 2.910 | 0.004 | 0.635,3.304 |
| logT2D course:log transformation of T2D course;logN-MID:log transformation of N-MID;logβ-CTX:log transformation of β-CTX. | ||||||
本次研究中,我们初步探索了骨代谢指标:25(OH)D、β-CTX、N-MID、Ca及P与HbA1c之间的关系。考虑到骨代谢中存在的性别相关差异,我们将患者分为男女亚组,探索不同性别中骨代谢指标与HbA1c的相关性。在不同HbA1c水平分组中,25(OH)D、β-CTX、Ca、P指标差异无统计学意义,仅N-MID指标差异有统计学意义。相关性分析也显示N-MID与HbA1c呈负相关,随着体内N-MID水平的升高,HbA1c水平下降。多元线性回归显示在排除年龄及BMI影响后,女性患者中病程和N-MID为HbA1c的影响因素,而在男性患者中,病程、N-MID和β-CTX为HbA1c的影响因素;与男性患者相比,N-MID与HbA1c的关联在绝经后T2D女性患者中更为显著。性激素是影响骨代谢的重要因素之一,破骨细胞具有雌激素受体,但没有雄激素受体。此外,绝经后女性的性激素水平较男性在同一更年期迅速下降。而雌激素对破骨细胞、成骨细胞和骨细胞具有直接活性,其主要作用是减少破骨细胞数量和功能。雌激素缺乏时,成骨细胞活性受损,对破骨细胞的抑制作用减弱,从而导致骨转换增加,骨形成和骨吸收失衡。与男性更年期后相比,女性通常会出现严重的绝经后症状[4-5]。
一项相似研究分析了T2D男性患者HbA1c水平与骨代谢指标的相关性,发现HbA1c与OC呈负相关(r=-0.162,P=0.002),而与25(OH)D、β-CTX无相关性[6]。同样地,在绝经后女性及老年T2D患者中,OC与HbA1c呈负相关。OC对患者的胰岛素敏感性及分泌功能具有积极的调控作用[2-3]。此次研究中我们发现N-MID与HbA1c水平呈负相关。N-MID为N端中段骨钙素,因其灵敏度高、稳定性好,是临床上常用的检测OC的形式[7]。血清OC包括羧化骨钙素和羧化下骨钙素(uncarboxylated osteocalcin,ucOC)[8]。ucOC作为一种激素诱导胰岛素分泌的药物,可用于糖尿病的治疗。胰腺β细胞是ucOC作用的主要靶点之一。ucOC能够通过增加胰岛β细胞的胰岛素分泌以及增强外周组织胰岛素敏感性来调节全身能量代谢,在OC缺乏的小鼠中,血液循环中胰岛素分泌、β细胞数量、β细胞增殖和胰腺胰岛素含量明显降低[9]。除了直接影响胰腺β细胞外,ucOC还可以通过刺激小肠分泌胰高血糖素样肽-1(glucagon-likepeptide-1,GLP-1)间接促进胰岛素分泌[10]。
许多研究开始探索OC在人体中的功能。到目前为止,绝大多数采用了横断面设计来研究循环总OC水平和/或ucOC水平与糖代谢改变之间的关系。这些研究表明,OC水平与空腹血糖、空腹胰岛素、胰岛素抵抗、BMI和高脂血症呈负相关[11-14]。未治疗的糖尿病患者和糖尿病前期患者的ucOC水平降低,而较高的血清ucOC水平与较高的HOMA-β相关,这是胰岛β细胞功能增强的表现[15-16]。此次研究中,我们发现在中老年T2D患者中,N-MID与HbA1c呈显著负相关,N-MID升高可能有助于T2D患者血糖控制。随着T2D患者N-MID水平的升高,HbA1c逐渐降低,提示以提高N-MID为目的骨质疏松的治疗,可能有助于T2D患者血糖的控制,也可以为将来开发T2D治疗药物提供新的方向。我们将来会围绕此研究展开一些临床试验。
随着基础和临床科研的深入,我们对骨骼生理学的理解在逐渐转变。骨骼是人体最大的器官系统之一,约占总体重的15%。传统上,它被认为是一种支持身体运动和保护内脏器官的结构性器官。然而,越来越多的研究表明,骨骼也可能是一个活跃的内分泌器官,显然,骨钙素现在可以被视为一种骨源性因子,具有强大的胰岛素促分泌剂的功能,由于口服外源性ucOC可以有效地改善提高胰岛素的分泌,加强葡萄糖水平的控制,未来有望作为一种调节糖代谢的药物。
作者贡献声明 刘聪颖 文献调研与整理,论文撰写与修订。潘俊宏 可行性分析,数据搜集与整理。文松 数据分析,图表绘制。周里钢 论文构思与设计,指导、修订与审核。
利益冲突声明 所有作者均声明不存在利益冲突。
| [1] |
VESTERGAARD P. Discrepancies in bone mineral density and fracture risk in patients with type 1 and type 2 diabetes--a meta-analysis[J]. Osteoporos Int, 2007, 18(4): 427-44.
[DOI]
|
| [2] |
许小娟, 李华. 绝经后女性2型糖尿病患者骨钙素与糖化血红蛋白的相关性研究[J]. 中国医药科学, 2021, 11(2): 6-9. [CNKI]
|
| [3] |
苏晓慧, 李维辛. 骨钙素在老年2型糖尿病患者中的血糖调控作用及其影响因素研究[J]. 中国全科医学, 2020, 23(17): 2157-2163. [CNKI]
|
| [4] |
PINES A. Male menopause: is it a real clinical syndrome?[J]. Climacteric, 2011, 14(1): 15-17.
[DOI]
|
| [5] |
GOULD DC, PETTY R, JACOBS HS. For and against: The male menopause--does it exist?[J]. BMJ, 2000, 320(7238): 858-861.
[DOI]
|
| [6] |
阴树苓, 崔建娇. 2型糖尿病男性患者糖化血红蛋白水平与骨代谢标志物的相关性[J]. 中国现代医学杂志, 2020, 30(22): 71-74. [CNKI]
|
| [7] |
NAGASUE K, INABA M, OKUNO S, et al. Serum N-terminal midfragment vs. intact osteocalcin immunoradiometric assay as markers for bone turnover and bone loss in hemodialysis patients[J]. Biomed Pharmacother, 2003, 57(2): 98-104.
[DOI]
|
| [8] |
POSER JW, ESCH FS, LING NC, et al. Isolation and sequence of the vitamin K-dependent protein from human bone. Undercarboxylation of the first glutamic acid residue[J]. J Biol Chem, 1980, 255(18): 8685-8691.
[DOI]
|
| [9] |
LEE NK, SOWA H, HINOI E, et al. Endocrine regulation of energy metabolism by the skeleton[J]. Cell, 2007, 130(3): 456-469.
[DOI]
|
| [10] |
MIZOKAMI A, YASUTAKE Y, GAO J, et al. Osteocalcin induces release of glucagon-like peptide-1 and thereby stimulates insulin secretion in mice[J]. PLoS One, 2013, 8(2): e57375.
[DOI]
|
| [11] |
HWANG YC, JEE JH, JEONG IK, et al. Circulating osteocalcin level is not associated with incident type 2 diabetes in middle-aged male subjects: mean 8.4-year retrospective follow-up study[J]. Diabetes Care, 2012, 35(9): 1919-1924.
[DOI]
|
| [12] |
KINDBLOM JM, OHLSSON C, LJUNGGREN O, et al. Plasma osteocalcin is inversely related to fat mass and plasma glucose in elderly Swedish men[J]. J Bone Miner Res, 2009, 24(5): 785-791.
[DOI]
|
| [13] |
YEAP BB, CHUBB SA, FLICKER L, et al. Reduced serum total osteocalcin is associated with metabolic syndrome in older men via waist circumference, hyperglycemia, and triglyceride levels[J]. Eur J Endocrinol, 2010, 163(2): 265-272.
[DOI]
|
| [14] |
CHEN X, WU Y, LIU L, et al. Osteocalcin is inversely associated with glucose levels in middle-aged Tibetan men with different degrees of glucose tolerance[J]. Diabetes Metab Res Rev, 2014, 30(6): 476-482.
[DOI]
|
| [15] |
HWANG YC, JEONG IK, AHN KJ, et al. The uncarboxylated form of osteocalcin is associated with improved glucose tolerance and enhanced beta-cell function in middle-aged male subjects[J]. Diabetes Metab Res Rev, 2009, 25(8): 768-772.
|
| [16] |
SARKAR PD, CHOUDHURY AB. Relationships between serum osteocalcin levels versus blood glucose, insulin resistance and markers of systemic inflammation in central Indian type 2 diabetic patients[J]. Eur Rev Med Pharmacol Sci, 2013, 17(12): 1631-1635.
|
 2022, Vol. 49
2022, Vol. 49


