前列腺癌是老年男性常见的恶性肿瘤之一, 据2018年统计显示, 它是西方男性最常见的恶性肿瘤, 在肿瘤相关死亡中位列第二[1]。我国前列腺癌的发病率低于西方国家, 但最近10多年呈上升态势, 已成为威胁我国男性健康的重要疾病之一[2-3]。为了更系统和全面地开展前列腺癌研究, 自2003年1月起复旦大学附属中山医院泌尿外科开发和建立了本院前列腺癌住院患者数据库。本文回顾性分析2003年1月至2012年12月的前列腺癌患者住院病例1 673例, 分为2003—2007年(前5年)与2008—2012年(后5年)两个连续5年的时间段, 分析比较患者的初诊疾病基线状态和接受治疗方式的变化, 探讨前列腺癌在上海单中心的诊治、患者生存情况及其相关预后因素, 以提高前列腺癌的防治水平。
资料和方法研究对象 收集2003—2012年我院收治的所有前列腺癌患者1 673例。其中, 上海市市区(包括原黄浦、卢湾、徐汇、长宁、静安、普陀、闸北、虹口和杨浦9个市区)患者901例。本组患者年龄44~96岁, 平均年龄(71.9±7.9)岁。按时间顺序分组, 将患者分为2组:2003—2007年(n=542)为第1组, 2008—2012年(n=1 131)为第2组。本次研究采用电话结合信件的方式进行随访, 随访截至2014年12月31日。
研究方法 患者均经前列腺穿刺活检或转移灶的病理明确诊断。收集前列腺癌住院患者数据库中临床资料包括初诊年龄、初诊前列腺特异性抗原(prostate specific antigen, PSA)、穿刺活检病理Gleason总评分(Gleason-sum score, GS)、TNM分期(根据2002年AJCC前列腺癌TNM分期[4]、治疗方式及患者生存状态。治疗方式包括根治性前列腺切除术、I125放射性粒子永久性植入前列腺(内放疗)、去势手术(指双侧睾丸切除术), 外放疗(radiotherapy, RT)和高强度聚焦超声(high intensity focused ultrasound, HIFU)。根治性前列腺切除手术方法分为开放手术(open radical prostatectomy, ORP)、腹腔镜手术(laparoscopic radical prostatectomy, LRP)和机器人辅助手术(robot-assisted radical prostatectomy, RARP)(表 1)。
| [n (%)*] | ||
| Parameters | 2003-2007 (n=542) |
2008-2012 (n=1 131) |
| Diagnosis age (y) (P=0.003) | 71.9±7.8 | 70.8±8.0 |
| Presenting PSA (ng/mL)(P=0.004)a | ||
| <20 | 139 (32.9) | 361 (38.1) |
| ≥20, < 100 | 145 (34.4) | 360 (37.9) |
| ≥100 | 138 (32.7) | 228 (24.0) |
| TNM staging (AJCC, 2002) (P<0.000 1)a | ||
| Ⅰ-Ⅱ | 112 (41.0) | 390 (53.7) |
| Ⅲ | 11 (4.0) | 38 (5.2) |
| Ⅳ | 150 (55.0) | 299 (41.1) |
| Site of metastasis (P0.05)a | ||
| Soft tissue onlyb | 17 (11.4) | 37 (12.4) |
| Bone only | 113 (75.8) | 201 (67.7) |
| Soft tissue and bone | 19 (12.8) | 59 (19.9) |
| Biopsy GS (P=0.012)a | ||
| <7 | 121 (28.3) | 214 (20.9) |
| =7 | 126 (29.5) | 328 (32.0) |
| >7 | 180 (42.2) | 482 (47.1) |
| Treatment strategies (P<0.000 1)a | ||
| Radical prostatectomy | 77 (14.2) | 381 (33.7) |
| I125 brachytherapy | 17 (3.1) | 69 (6.1) |
| Surgical castration | 414 (76.4) | 605 (53.5) |
| Surgical castration plus local therapy (external radiotherapynd/or HIFU) | 34 (6.3) | 76 (6.7) |
| RP approach (P<0.000 1)a | ||
| ORP | 73 (94.8) | 238 (62.5) |
| LRP | 4 (5.2) | 64 (16.8) |
| RARP | 0 | 79 (20.7) |
| *Ratio referred to the proportion of subgroup patients out of the group patients.aP value represented the difference in proportion of subgroups between two groups.bSoft tissue included non-regional lymph nodes and visceral organs. | ||
10年间, 我院收治前列腺癌患者数逐年增加, 从2003年全年收治前列腺癌患者71例, 到2005年之后持续每年超过100例, Mann-kendall趋势检验显示呈显著上升趋势(P=0.000 3)。2008—2012年为1 131例, 较2003—2007年542例, 增加589例, 增长109%。所有患者中, 1 371例(81.9%)有可查询的初诊PSA值, 1 000例(59.8%)有初诊时可供临床分期的影像学资料, 1 451例(86.7%)有确切的穿刺活检病理GS。2组患者的疾病基线情况比较(表 1), 包括初诊年龄、初诊PSA、穿刺活检病理GS、临床分期和转移区域分布, 2组的治疗方式有显著变化(P < 0.000 1)。由于2013—2017年手术患者随访数据尚不完整, 而没有放入此次研究的统计中, 事实上2013年以后治疗方式的构成比又发生了进一步变化。根据初步统计, 2013—2015年前列腺癌患者共885例, 其中根治术、内放疗及去势手术数量占所有治疗的比例分别为62.7% (555例)、2.3% (20例)和35.0% (310例)。显然, 根治术的比例显著增加, 并且我院2009年7月开始施行RARP手术, 临床上已占主导地位, RARP、LRP及ORP手术量占根治术比例分别为54.6% (303例)、13.9% (77例)和31.5% (175例)。
统计学分析 应用Stata 13.0软件统计分析2个时间段的患者资料, 组间比较计量资料采用t检验, 计数资料采用χ2检验, 等级资料采用Mann-Whitney U检验。运用Kaplan-Meier估算法生成总体生存曲线。Mann-kendall趋势检验评估每年收治病例数变化。采用单因素和多因素Cox模型计算不同亚组疾病基线状态对生存的影响。P < 0.05为差异有统计学意义。
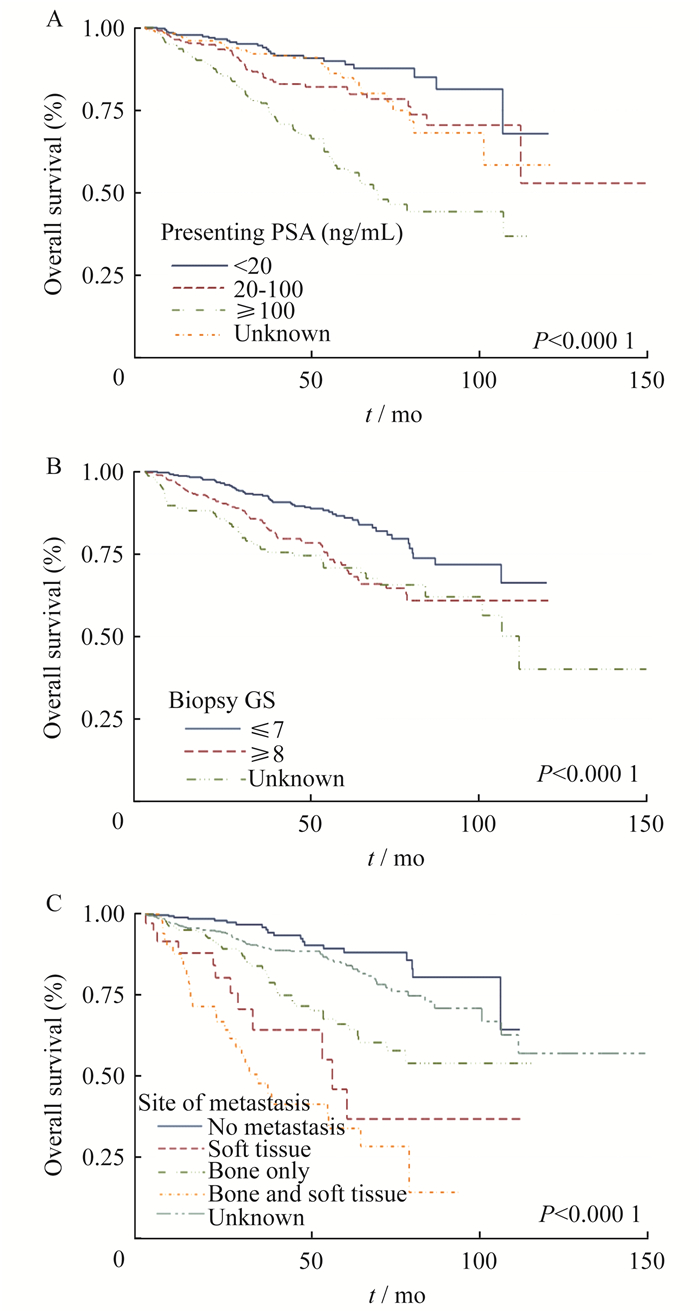
结果入组患者中随访955名(占57.1%), 中位随访28(1~121)个月, 1、3和5年生存率分别为96.0%、87.3%和78.9%。第1组和第2组患者的1、3和5年生存率比较, 分别为96.2% vs.95.6%, 87.6% vs.87.0%和79.2% vs.73.5%, 2组间差异均无统计学意义(P=0.68)。综合所有随访患者, 进一步按患者疾病的初诊基线情况进行生存分析。表 2显示了各个可能因素对总体生存(overall survival, OS)的相对风险比。在控制了年龄因素的单因素模型中, 疾病相关指标如血清PSA水平(P < 0.001)、穿刺活检病理GS (P < 0.001)和转移部位(P < 0.001)均与OS相关。多因素模型中, 年龄(P < 0.001)、血清PSA高水平(P=0.012)、穿刺活检病理GS高评分(P=0.006)和存在远处转移(P < 0.001)均是OS的独立风险因素。图 1分别展示了不同PSA水平、穿刺活检病理GS、转移部位和治疗方式的Kaplan-Meier曲线。PSA < 20 ng/mL, 20~100 ng/mL以及≥100 ng/mL患者的5年生存率分别为88.8%, 81.0%和56.1%。GS≤7以及≥8患者的5年生存率分别为86.1%和71.7%。局限性前列腺癌、仅软组织转移、仅骨转移以及骨和软组织转移患者的5年生存率分别为88.2%、36.7%、66.1%和33.9%。接受根治性手术、I125放射性粒子植入治疗、单纯内分泌治疗、内分泌治疗联合局部治疗(放疗或HIFU作为辅助治疗或补救治疗)患者的5年生存率分别为91.9%、94.2%、75.1%和62.1%。在接受根治术的患者中, 接受开放根治性手术和腹腔镜根治性手术(包括LRP和RARP)患者的5年生存率分别为91.5%和99.0%, 两者差异无统计学意义。
| Parameters | Univariate analysisa | Multivariate analysisb | |||||
| HR | 95% CI | P | HR | 95% CI | P | ||
| Age | 1.05 | 1.03-1.07 | <0.001 | ||||
| Diagnosis period | 0.60 | ||||||
| 2003-2007 | 1.00 | ||||||
| 2008-2012 | 1.08 | 0.74-1.57 | |||||
| PSA level (ng/mL) | <0.001 | 0.012 | |||||
| <20 | 1.00 | 1.00 | |||||
| ≥20, <100 | 1.89 | 1.17-3.07 | 1.41 | 0.85-2.34 | |||
| ≥100 | 4.23 | 2.71-6.60 | 1.98 | 1.16-3.38 | |||
| unknown | 1.44 | 0.84-2.47 | 1.04 | 0.59-1.85 | |||
| Biopsy GS | <0.001 | 0.006 | |||||
| ≤7 | 1.00 | 1.00 | |||||
| ≥8 | 2.07 | 1.47-2.91 | 1.50 | 1.05-2.14 | |||
| unknown | 2.55 | 1.71-3.82 | 1.80 | 1.18-2.73 | |||
| Site of metastasis | <0.001 | <0.001 | |||||
| No metastasis | 1.00 | 1.00 | |||||
| Soft tissue only | 6.65 | 3.25-13.63 | 4.04 | 1.88-8.68 | |||
| Bone only | 3.21 | 1.89-5.43 | 1.90 | 1.04-3.46 | |||
| soft tissue and bone | 10.49 | 5.89-18.69 | 5.91 | 3.05-11.42 | |||
| unknown | 1.53 | 0.92-2.54 | 1.28 | 0.75-2.19 | |||
| HR:Hazard ratio; CI:Confidence interval; aUnivariate analysis referred to the age-adjusted cox mode; bMultivariate analysis referred to the all factors considered cox model. | |||||||
|
| A:Serum PSA level at diagnosis; B:Biopsy Gleason score; C:Site of metastasis. 图 1 不同分层情况下前列腺癌患者Kaplan-Meier总体生存曲线比较 Fig 1 Kaplan-Meier curves of overall survival for patients with prostate cancer using various stratifications |
前列腺癌是西方国家男性的高发恶性肿瘤, 我国属低发病地区, 但是随着我国社会人口老龄化加快, 环境、饮食等因素的改变, 以及PSA筛查的普及, 近10多年我国尤其是经济较发达城市的前列腺癌发病率正在显著上升[5]。据统计, 上海市市区男性前列腺癌发病率已由1984年的1.8/10万人逐年上升至2011年的36.67/10万人[3]。本研究结果显示, 我院收治住院的前列腺癌患者病例数由2003—2007年的542例增至2008—2012年的1 131例, 增长109%。这尚未包括门诊接受药物去势治疗的前列腺癌患者。由于近几年药物去势治疗被越来越多的中国医师和患者所接受, 我科后5年接诊的前列腺癌患者较前5年实际增加更多。此文主要关注的是自2003年我科建立前列腺癌数据库后10年的病例数据, 近5年就诊的前列腺癌患者又有进一步增加。由于这部分患者随访数据尚未完善, 将在后续报道予以更新。
由于肿瘤二级预防意识的增强, PSA筛查的普及和早期诊断水平提高, 不仅增加了前列腺癌患者的检出率, 也使患者诊断时的基线疾病状态发生了变化。首先, 后5年患者的平均年龄较前5年降低了1岁[(71.9±7.8)岁vs.(70.8±8.0)岁], 这一变化趋势与美国类似, 患者的平均诊断年龄由PSA时代(20世纪90年代早期起)之前的70岁降低至此后的67岁[6]。其次, 诊断时肿瘤分期在患者中的分布比例也发生了变化, 后5年患者就诊时为局限性前列腺癌患者, 占比达58.9%。在前5年中这一比例仅为45.0%, 而就诊时为转移性前列腺癌, 却占比达55.0%。发生远处转移的患者中, 转移部位的分布并无显著差异, 骨转移仍然是最常见的转移部位, 这与西方国家的大样本报道一致[7]。另外, 肿瘤病理分级的变化也显示出差异。美国SEER (Surveillance, Epidemiology and End Results)数据库资料显示[8], 1984—2003年诊断时肿瘤病理分级有显著的演变趋势, 主要表现为由高分化肿瘤转变为中分化的肿瘤。本研究结果显示, 后5年诊断的患者中GS≥7的2个亚组患者比例均较前5年增加。PSA筛查后前列腺癌发病率增加的问题曾经引发医学界的担忧, 认为它仅仅多发现了临床意义不大的低危前列腺癌。然而, 美国20年间以及我院10年间的数据均显示, 前列腺癌病例增加更多的却是中高危前列腺癌患者人群。
在OS方面, 后5年病例的OS并未如预期显著高于前5年, 可能是由于2组间的差异不足以在5年内体现出来, 需要等待10年或者更长时间随访后的进一步比较; 也可能由于后5年的随访时间短于前5年, 造成统计的生存时间有差异, 但是统计模型会考虑到这些影响因素, 所以两个时间段的差异无统计学意义(P=0.60)。此外, 也有可能由于后5年患者中GS高分患者更多, 且近些年我国患者就诊区域流动性增加, 一部分非本地区的高危病例加入了后5年的统计。尽管如此, 综合分析10年间的病例资料, 我们认为:(1)肿瘤基线特征对OS的影响。结果显示高PSA、高GS和有远处转移均是OS的独立风险因素。初诊PSA>100 ng/mL患者的死亡风险是<20 ng/mL患者的4.23倍; 原发肿瘤穿刺活检病理GS≥8患者是GS≤7患者的2.07倍; 初诊时同时有骨和软组织转移的患者, 其死亡风险分别是仅软组织转移、仅骨转移和无转移患者的6.65倍、3.21倍和10.49倍。(2)不同治疗方式对OS的影响。由于不同治疗方式适应的患者人群不同, 其本身的生存状况存在差异, 于是通过在同一类型患者中进行比较, 结果显示:在局限性前列腺癌患者中, 根治性手术与I125放射性粒子植入治疗对OS无显著差异(91.9% vs.94.2%); 根治性手术的不同方式也对OS无显著差异(开放手术91.5% vs.腹腔镜手术99.0%)。据报道, 日本地区的根治性前列腺切除术患者的5年OS为83.5%[9], 而北美地区则分别有报道为87.4%[10]、93%[11]和96%[12]。在I125放射性粒子植入治疗方面, 我院自2002年6月起开展此项治疗, 早期经验已经显示其良好的近期疗效和安全性[13], 而文献报道其5年OS为85%~96.4%[14-16]。内分泌治疗主要适合晚期前列腺癌患者, 本研究结果显示, 接受内分泌联合局部治疗患者的OS较单纯内分泌治疗者低, 这是由于两部分患者人群并不对等, 单纯内分泌组包括了不同年龄层次的高、中、低危肿瘤, 而联合治疗组大部分为晚期高危肿瘤。然而, 我院曾报道一组120例局部进展期前列腺癌治疗结果, 其中内分泌治疗后补充HIFU+低剂量外放疗相较于单纯内分泌治疗, 患者的5年生存率提高了1倍(69.92% vs.34.43%)[17], 该治疗方案利用HIFU对前列腺肿瘤局部造成凝固性坏死, 同时外放疗对前列腺周围及盆腔淋巴结可能的微转移灶进行控制, HIFU和放疗的协同效应以及HIFU对机体产生的免疫效应能够有效提高患者的总体生存[18]。
目前局限性前列腺癌最有效的治疗手段仍是根治性前列腺切除术。传统的开放手术创伤大, 且易发生如尿失禁、尿道狭窄、勃起功能障碍等并发症, 影响患者的预后和生存[5]。Da Vinci机器人外科手术系统是2000年由美国FDA批准正式应用于临床的新一代机器人辅助腹腔镜外科手术系统。它拥有放大的高清晰度三维视野, 独特设计的内腕具有7个自由度和540度旋转以及符合人体工程学设计的操作台, 这些使RARP不仅具有传统腹腔镜的微创优势, 还克服了传统腹腔镜操作难度大、视野清晰度不足、学习曲线长的不足。国内外的报道均显示, 在克服早期学习曲线后, RARP具有手术时间缩短、出血少、术后恢复快、尿失禁发生率低等优势[19-21]。
本研究尚存在一些不足:(1)由于患者的就诊流动性比较大, 生存分析的随访率为57.1%, 研究结果不能够全面地反映患者情况, 但该随访率与生存结果无关, 仅与是否能获得随访有关, 所以本研究还是具有一定的客观性; (2)本中心是上海及国内较大的泌尿男生殖系肿瘤诊疗中心之一, 研究数据具有代表性, 但尚不能完全反映全国前列腺癌患者及其诊治的变化趋势, 有待今后多中心进一步研究。
本研究结果显示, 10多年来我国前列腺癌诊治人数呈明显上升, 同时初诊患者平均年龄降低。局限性前列腺癌、中低分化(GS≥7)肿瘤分级以及初诊PSA < 20 ng/mL的患者占比显著增加。研究表明, 高PSA、高GS、有远处癌转移均是患者OS的独立风险因素。由于局限性前列腺癌患者增加, 临床开展根治性手术越来越普及, 采用机器人辅助手术已经显示其独特的优点, 在中国已装备机器人的医院里正在逐渐取代开放手术和传统腹腔镜手术。
致谢 张健、王一惟、王佳骏医师在病历资料收集和患者查询等方面给予帮助。
| [1] |
SIEGEL RL, MILLER KD, JMAL A, et al. Cancer statistics, 2018[J]. CA Cancer J Clin, 2018, 68(1): 7-30.
[DOI]
|
| [2] |
齐金蕾, 王黎君, 周脉耕, 等. 1990—2013年中国男性前列腺癌疾病负担分析[J]. 中华流行病学杂志, 2016, 37(6): 778-782. [DOI]
|
| [3] |
上海市疾病预防控制中心. 2011年上海市市区恶性肿瘤发病率[J]. 肿瘤, 2015, 35(7): 附录Ⅰ. [CNKI]
|
| [4] |
AMERICAN JOINT COMMITTEE ON CANCER. AJCC cancer staging manual (6th ed)[M]. New York: Springer, 2002: 309-317.
|
| [5] |
孙颖浩. 前列腺癌诊治进展[J]. 上海医学, 2011, 34(7): 487-488. [DOI]
|
| [6] |
BRAWLEY OW. Prostate cancer epidemiology in the United States[J]. World J Urol, 2012, 30(2): 195-200.
[DOI]
|
| [7] |
JAMES ND, SPEARS MR, CLARKE NW, et al. Survival with newly diagnosed metastatic prostate cancer in the "docetaxel era":data from 917 patients in the control arm of the STAMPEDE trial (MRC PR08, CRUK/06/019)[J]. Eur Urol, 2015, 67(6): 1028-1038.
[DOI]
|
| [8] |
JANI AB, MASTER VA, ROSSI PJ, et al. Grade migration in prostate cancer:an analysis using the surveillance, epidemiology, and end results registry[J]. Prostate Cancer Prostatic Dis, 2007, 10(4): 347-351.
[URI]
|
| [9] |
HACHIYA T, OKADA Y, KAWATA N, et al. Long-term survival following radical prostatectomy in Japanese men with clinically localized prostate cancer:a single institutional study[J]. Int J Urol, 2004, 11(10): 862-869.
[DOI]
|
| [10] |
PIERORAZIO PM, GUZZO TJ, HAN M, et al. Long-term survival after radical prostatectomy for men with high gleason sum in pathologic specimen[J]. Urology, 2010, 76(3): 715-721.
[DOI]
|
| [11] |
ABDOLLAH F, SUN M, SCHMITGES J, et al. Cancer-specific and other-cause mortality after radical prostatectomy versus observation in patients with prostate cancer:competing-risks analysis of a large North American population-based cohort[J]. Eur Urol, 2011, 60(5): 920-930.
[DOI]
|
| [12] |
BOORJIAN SA, KARNES RJ, RANGEL LJ, et al. Mayo Clinic validation of the D'amico risk group classification for predicting survival following radical prostatectomy[J]. J Urol, 2008, 179(4): 1354-1360.
[DOI]
|
| [13] |
王国民, 徐志兵, 朱延军, 等. 125I放射性粒子永久植入治疗前列腺癌[J]. 中华泌尿外科杂志, 2005, 26(4): 263-266. [DOI]
|
| [14] |
BATTERMANN JJ, BOON TA, MOERLAND MA. Results of permanent prostate brachytherapy, 13 years of experience at a single institution[J]. Radiother Oncol, 2004, 71(1): 23-28.
[URI]
|
| [15] |
AALTOMAA SH, KATAJA VV, LAHTINEN T, et al. Eight years experience of local prostate cancer treatment with permanent I125 seed brachytherapy--morbidity and outcome results[J]. Radiother Oncol, 2009, 91(2): 213-216.
[DOI]
|
| [16] |
OHASHI T, YOROZU A, SAITO S, et al. Outcomes following iodine-125 prostate brachytherapy with or without neoadjuvant androgen deprivation[J]. Radiother Oncol, 2013, 109(2): 241-245.
[DOI]
|
| [17] |
WU RY, WANG GM, XU L, et al. The feasibility and safety of high-intensity focused ultrasound combined with low-dose external beam radiotherapy as supplemental therapy for advanced prostate cancer following hormonal therapy[J]. Asian J Androl, 2011, 13(3): 499-504.
[DOI]
|
| [18] |
徐磊, 王国民, 武睿毅, 等. 高强度聚焦超声对手术去势后前列腺癌患者抗肿瘤免疫功能的影响[J]. 复旦学报(医学版), 2009, 36(5): 538-542. [DOI]
|
| [19] |
FICARRA V, NOVARA G, ARTIBANI W, et al. Retropubic, laparoscopic, and robot-assisted radical prostatectomy:a systematic review and cumulative analysis of comparative studies[J]. Eur Urol, 2009, 55(5): 1037-1063.
[DOI]
|
| [20] |
孙立安, 王国民, 徐志兵, 等. 机器人辅助腹腔镜根治性前列腺切除术130例[J]. 中华腔镜外科杂志(电子版), 2013, 6(5): 357-361. [URI]
|
| [21] |
王国民. 前列腺癌机器人辅助手术的现状与展望[J]. 肿瘤防治研究, 2017, 44(10): 643-646. [DOI]
|
 2019, Vol. 46
2019, Vol. 46


